Povećana hemostaza. Potpuno izlečenje se ne dešava. Sva terminalna stanja, srčani zastoj

Pacijent sa skorbutom ima krvarenje desni i petehije na koži. Šta uzrokuje poremećenu hemostazu u ovoj bolesti?
A. @ Kršenje sinteze kolagena
B. Trombocitopenija
C. Višak antikoagulansa
D. Aktivacija fibrinolize
E. Nedostatak prokoagulanta
Dečak sa hemoragičnim sindromom nema antihemofilni globulin A u krvi (faktor VIII). Koji mehanizam hemokagulacije ima ovaj pacijent?
@ Unutarnji mehanizam formiranja protrombinaze
Pretvaranje fibrinogena u fibrin
Spoljni mehanizam formiranja protrombinaze
Konverzija protrombina u trombin
Povlačenje krvnog ugruška
Čovjek koji je dvije godine bolovao od kronične mijeloidne leukemije, primljen je u bolnicu u stanju akutnog zatajenja bubrega. Šta može biti uzrok akutnog zatajenja bubrega kod ovog pacijenta?
@DIC - sindrom
Limfopenija
Neutropenija
Trombocitopenija
Nedovoljna aktivnost bilo kojih faktora zgrušavanja uzrokuje razvoj hemoragijskog sindroma kod pacijenata sa hipovitaminozom K?
@ X, IX, VII, II
Von Willebrandov faktor
Pacijent koji je sistematski konzumirao acetilsalicilnu kiselinu razvio je krvarenje. Sa smanjenjem aktivnosti kod kojih su trombocitni enzimi povezani sa razvojem trombocitopatije u ovom slučaju?
@ Ciklo-oksigenaza
Lipooxygenase
Peroksidaza
Citokrom oksidaza
Glukoza - 6 - fosfat dehidrogenaza
Djevojka povremeno krvari iz nosa, na koži se javlja mali hemoragični osip. Pregledom je utvrđeno: vreme krvarenja - 10 minuta, smanjena sposobnost adhezivnih trombocita i niska aktivnost f. VIII (VIII: C). Koja je bolest kod deteta?
@ Von Willebrand bolesti
Hemofilija A
Hemofilija B
Hereditary Dysfibrinogenemia
Trombocitopenija
Nakon što je pretrpjela upalu grla, 5-godišnja djevojčica ima petehijski osip na koži torza i ekstremiteta, krvareći iz desni. Pregledom je utvrđeno smanjenje broja trombocita u krvi. Na kojem nivou trombocitopenije (g / l) se pojavljuju njeni klinički znaci?
Šta bi mogla biti glavna karika u patogenezi trombofilije kod pacijenta koji pati od tromboflebitisa donjih ekstremiteta?
@ Nedostatak antikoagulansa
Trombocitopenija
Trombocitopatija
Nedostatak prokoagulanta
Da bi se dijagnosticirala promena u sistemu hemokagulacije propisana je studija o nivou produkata degradacije fibrina u krvi?
Trombocitopatija
Trombocitopenija
Vasopathy hemorrhagic
Pacijentu je dijagnosticiran genetski defekt membranskog receptora za von Willebrandov faktor - glikoprotein (GP) Ib, koji je odgovoran za početnu fazu adhezije trombocita na kolagen. Kako se zove ova bolest?
@ Bernard - Soulier
Von Willebrand
Addison - Birmera
Wilson - Konovalova
Glantsmana - Negeli
Pacijentu je dijagnosticiran nasljedni defekt GP IIb - IIIa - membranski receptor koji osigurava vezu fibrina s membranom trombocita i potreban je za njihovu agregaciju. O kojoj bolesti govorimo?
@Glancman - Negeli
Von Willebrand
Addison - Birmera
Wilson - Konovalova
Bernard - Soulier
Kod deteta sa kombinovanom imunodeficijencijom, krvni test je pokazao smanjenje adhezije trombocita na kolagen, njihovu agregaciju, slabljenje zgrušavanja krvi i retrakciju krvnog ugruška. Pod kojom imunodeficijencijom su uočene slične promjene?
@ Whiskott - Aldrich
Swiss type
Di - Georgie
Nezelofa
Bolesnoj djevojci dijagnosticirana je Glantsmanova trombastenija. Kakvo je oštećenje hemostatskog sistema?
@Disaggregation thrombocytopathy
Absolute Thrombocytopenia
Disashezivna trombocitopatija
Nedovoljna trombocitopatija
Distegranulacijska trombocitopatija
Članovi ekspedicije koji su bili na sjeveru žale se na krvarenje gingive i petehijalna krvarenja na koži. Iz anamneze je poznato da ishrana nije imala dovoljno askorbinske kiseline, a to je dovelo do krhkosti vaskularnog zida. Šta je patogeneza vazopatije?
@ Displastic
Inflamatory
Metaplastic
Dystrophic
Imuni
Kod pacijenta nakon duge operacije na pankreasu, postoperativna rana je dugo krvarila. Prema koagulogramu utvrđeno je značajno povećanje nivoa plazmina. Koji je patogeneza koagulopatije u ovom slučaju?
@ Fibrinopathy
Protrombinasopatija
Tromboplastinopatija
Trombinopatija
Vasopatija
Pacijentu je dijagnosticiran genetski defekt faktora V, koji postaje neosjetljiv na inaktivaciju antitrombotskog kompleksa trombomodulin - protein C, koji smanjuje sposobnost vaskularnog zida da ograniči stvaranje fibrina. Koja će patologija zgrušavanja krvi nastati sa ovom anomalijom?
@Thrombophilia
Trombocitopenija
Trombocitopatija
Hemorrhagic syndrome
Ključni koncepti oslabljene hemostaze:
1. Hemostatični poremećaji, koagulopatija (koagulopatija, koagulo + grčki. patos - patnja, bolest) - oštećena funkcija sistema zgrušavanja i koagulacije krvi.
2. Hiperkoagulativno trombotično stanje- stanje, praćeno patološkim procesom povećanog zgrušavanja krvi zbog povećane agregacije trombocita, aktivacije faktora koagulacije plazme i tkiva sa stvaranjem krvnih ugrušaka trombocita i fibrina.
3. Hipokagulativno hemoragijsko stanje- Stanje koje je praćeno patološkim procesom smanjenja zgrušavanja krvi zbog smanjenja agregacije trombocita, inaktivacije faktora zgrušavanja plazme i tkiva sa pojavom krvarenja i krvarenja.
4. DIC sindrom (trombotično hemoragično stanje) - sindrom diseminirane intravaskularne koagulacije krvi - tipičan patološki proces oštećenja hemostaze kao posljedica raka na moru distrofija unutrašnjih organa.
U kojim oboljenjima postoji kršenje hemostaze:Hemostaza je složen proces koji sprečava ili zaustavlja istjecanje krvi iz lumena posude, osigurava konvoluciju fibrina neophodnu za obnavljanje integriteta tkiva i konačno uklanja fibrin kada nestaje potreba za njim. Četiri glavna fiziološka mehanizma su uključena u ovaj proces.
Uz pomoć sistema hemostaze, krv obavlja svoju najvažniju funkciju - održavanje tekućeg stanja krvi koja teče u krvnim sudovima i koagulaciju krvi, čime se narušava integritet krvožilnog zida i time prestaje krvarenje i čuva se volumen i sastav krvi. Sistem hemostaze je višekomponentan. To uključuje trombocite i druge krvne ćelije, vaskularni zid, ekstravaskularno tkivo, biološki aktivne supstance (trombocitno-vaskularni hemostazu), plazmu, faktore koagulacije tkiva (koagulacijski hemostaz), koji su u bliskoj interakciji s antikoagulantima, fibrinolitikom i kalikreinom-kinovitinovim. Kršenje bilo koje od ovih komponenti dovodi do patologije hemostaze.
Klasifikacija poremećaja hemostaze. Patologija hemostaze se klasificira prema pretežnoj leziji njenih različitih komponenti na povrede vaskularne hemostaze trombocita i koagulacijske hemostaze. Prema etiologiji, ovi poremećaji mogu biti stečeni i nasljedni, a prema smjeru promjena podijeljeni su na smanjenje zgrušavanja krvi (hipokagulacija) i povećanje koagulacije krvi (hiperkoagulacija), što može biti lokalno (tromboza) i generalizirano (DIC).
Smanjenje zgrušavanja krvi
Smanjenje zgrušavanja krvi manifestuje se povećanim krvarenjem (hemoragijski sindrom) - ponovljenim krvarenjem, krvarenjem, koje nastaje spontano i sa lakšim povredama.
Trombocitno-vaskularna hemostaza poremećena je kvantitativnim i kvalitativnim promjenama u trombocitima (trombocitopenija i trombocitopatija), kao i lezije vaskularnog zida.
Trombocitopenija se naziva smanjenje broja trombocita u krvi ispod norme (180-320 G / l ili 180-320x109 / l). Međutim, spontano krvarenje se javlja samo kada njihov broj padne ispod 30 G / l. Pod trombocitopatijama razumiju kvalitet inferiornosti i disfunkcije trombocita sa normalnim ili smanjenim sadržajem.Uzroci niskog zgrušavanja krvi. Uzrok trombocitopenije je često imunološki odgovor kada se modifikuje antigenska struktura trombocita pod dejstvom virusa, lekovi, razvoj antitrombocitnih autoantitela (sa hroničnom limfocitnom leukemijom, idiopatska trombocitopenija), nekompatibilnost majčinih i fetalnih trombocita. Pored toga, razvija se trombocitopenija zbog poraza megakariocitnog izdanka koštane srži ionizirajućim zračenjem, hemikalijama ili njegovom zamjenom tumorskim metastazama, leukemijskim infiltratima. Smanjenje trombocitopoeze može biti posljedica nedostatka cijanokobalamina i folne kiseline, nasljednog defekta u formiranju trombocita (uključujući i one sa nedostatkom trombocitopoetina). Rezultati trombocitopenije mehanička oštećenja trombociti sa splenomegalijom, veštački srčani zalisci, kao i povećana potrošnja trombocita sa lokalnom i generalizovanom intravaskularnom koagulacijom krvi.
Etiološki faktori koji uzrokuju trombocitopatiju uključuju djelovanje toksičnih supstanci i lijekova (alkohol, acetilsalicilna kiselina), ionizirajuće zračenje, endogene metabolite (s uremijom, cirozom jetre); nedostatak cijanokobalamina, hormonalni poremećaji (hipotiroidizam). Postoje i genetski defekti u strukturi membrane i biohemijski sastav trombocita (nedostatak trombostenina, faktora 3, ATP, ADP, G-6-FDG, membranski receptori za faktore V, VIII, XI, itd.).U hemoragijskim vazopatijama, oštećenje vaskularnog zida, što dovodi do kršenja krvnih žila i krvarenja krvnih žila, uzrokovano je povećanom propusnošću zidova krvnih sudova i njegovim uništavanjem zbog narušavanja sinteze kolagena (uz nedostatak askorbinske kiseline, nasljedni defekti sinteze kolagena, pod dejstvom biološke sinteze kolagena; alergija), radiotoksini (radijacija), imunski hemoragični vaskulitis, smanjenje angiotrofne funkcije trombocita tokom trombocita Otvorite i thrombocytopathy, uništavanje leukemije infiltracije vaskularnog zida. Jedan od uzroka krvarenja je smanjenje proizvodnje vaskularnog zida endotela von Willebrandovog faktora - komponenta velikog molekula koagulacijskog faktora VIII-krvi (nasljedna von Willebrandova bolest). Ovaj faktor se nakuplja u trombocitima i oslobađa kada se degranulira.
Neophodan je za normalno prijanjanje trombocita na kolagenski zid, a bez njega trombocitni tromb nije formiran. Hemoragijski sindrom je takođe primećen kada je povećana membranska peroksidacija membranskih fosfolipida, zbog čega se sintetizira i izlučuje u endotelu prekomjerna količina moćnih inhibitora agregacije trombocita, prostaciklina. Osim toga, narušena neurogena i humoralna regulacija vaskularnog tonusa dovodi do smanjenja krvne žile u krvnom zglobu, što dovodi do nemogućnosti blokiranja malih krvnih sudova trombocitnim trombom.
Patogeneza niske koagulacije krvi. Postoje četiri glavna mehanizma trombocitopenije: smanjenje proizvodnje, povećano uništavanje, povećana potrošnja (tromboza), redistribucija trombocita.
Poremećaj hemostaze i razvoj krvarenja tokom trombocitopenije usled sledećih mehanizama:
- povećana mikrovaskularna permeabilnost za eritrocite i druge komponente krvi (krvarenje u dijapemiji) i krhkost krvnih žila usled distrofije zida kada je angiotrofična funkcija trombocita isključena;
- smanjenje adhezivne-agregacijske funkcije trombocita;
- kršenje reakcije oslobađanja trombocitnih faktora zgrušavanja krvi, ADP, serotonin, adrenalin, antiheparinski faktor, što dovodi do nedovoljnog formiranja trombocitnog tromba, odsustva vazospazma i usporavanja koagulacije;
- smanjenje retrakcije ugruška kao rezultat smanjenja aktivnosti kontraktilnog trombocitnog proteina, trombostenina (faktor trombocita 8).U patogenezi trombocitopatije mogu se razlikovati dva glavna mehanizma njihove pojave: proizvodnja patoloških trombocita u koštanoj srži i uništavanje trombocita u svim dijelovima krvnog sistema. Patogeneza trombocitno-vaskularne hemostaze sa trombocitopatijom je ista kao i kod trombocitopenije, jer je povezana sa onesposobljavanjem trombocitnih funkcija.
Povreda koagulacijske hemostaze, koja dovodi do razvoja krvarenja, može biti uzrokovana sljedećim faktorima:
- stečeno i nasljedno smanjenje ili izobličenje sinteze faktora koagulacije plazme i trombocita i komponenti kalikrein-kinin sistema;
- inhibicija ili povećana potrošnja ovih faktora;
- povećanje endogenih antikoagulanata;
- aktiviranje fibrinolitičkog sistema;
- predoziranje antikoagulansima, fibrinolitičkim i defibrinacijskim lijekovima. Sve ovo je u osnovi kršenja jedne od tri faze koagulacije krvi i retrakcije ugrušaka ili njihove kombinovane promjene.Uzroci kršenja prve faze zgrušavanja krvi - formiranje tromboplastina - je smanjenje proizvodnje faktora (IX, X) u patologiji jetre, formiranje antitijela na određene faktore (VIII, IX) kod bolesti s patogenezom autoimune komponente (leukemija, kolagenoza) ili predoziranje takvog univerzalnog antikoagulanta kao heparina. Poznati su genetski defekti u sintezi faktora VIII, IX i XI, čiji nedostatak leži u razvoju hemofilije (redom ovih faktora je hemofilija A, B i C).
Povreda druge faze koagulacije krvi - formiranje trombina - javlja se ne samo kod bolesti jetre, već i kod hipo-i avitaminoze K, kada sinteza u jetri faktora II, V, VII uključenih u ovu fazu također opada (kod mehaničke žutice, enteritisa, opsežnog resekcija tankog crijeva, medicinska disbakterioza). Mogu postojati imuni inhibitori faktora V, VII (na primjer, u liječenju streptomicina sa sulfatom), njihovo pojačano izlučivanje putem bubrega, nasljedni nedostatak (faktor V u parahemofiliji) ili inaktivacija komponentama antikoagulantnog sistema - antitrombin, heparin (s anafilaktičkim šokom, predoziranjem heparinom).
Hemoragijska dijateza povezana sa kršenjem treće faze koagulacije - faza stvaranja fibrina, javlja se kada sinteza fibrinogena u jetri, pluća zahvaćena patološkim procesom opada, ili kao rezultat nasljedne hipo-, afibrinogenemije i deficita faktora stabilizacije fibrina (faktor XIII). Međutim, značajno češće, povreda treće faze je posljedica povećane fibrinolize u traumi (operaciji) pluća, materice, gušterače; opekotina, šok. To je zbog povećanog protoka aktivatora profibrinolizina (plazminogena) u krvno tkivo, mikrobnih fibrinokinaza, aktivatora leuko- i eritrocita, komponenti sistema kalikrein-kinina i sistema komplementa heparinskog kompleksa sa fibrinogenom, profibrinolizinom i adrenalinom (ovi sistemi su korišćeni od strane imitanata. Kudryashov).
Patogeneza. Glavne karike u patogenezi hemoragijske dijateze, razvijene u suprotnosti sa bilo kojom od faza koagulacije krvi, su hronični gubitak krvi i njegove posljedice, kao i strukturne i funkcionalne promjene na mjestu krvarenja (u zglobovima, unutrašnji organi, kože i drugih tkiva).
Povećana koagulacija krvi
Povećanje koagulacije krvi manifestuje se lokalnom (trombozom) ili generaliziranom intravaskularnom koagulacijom krvi, na osnovu povrede krvno-krvnih žila i koagulacijske hemostaze.Hiperkoagulacija može biti posljedica:
- povećanje funkcionalne aktivnosti sistema zgrušavanja krvi zbog povećanog unosa prokoagulanata i aktivatora zgrušavanja krvi u krv;
- povećanje sadržaja trombocita u krvi;
- smanjenje antitromboznih svojstava vaskularnog zida;
- smanjenje aktivnosti antikoagulantnog sistema krvi;
- slabljenje fibrinolize.Generalizirana (diseminirana) intravaskularna koagulacija krvi (DIC) je teška povreda hemostaze, koja se javlja kada se prokoagulanti i aktivatori koagulacije krvi prekomjerno ubrizgaju u krvotok, što dovodi do formiranja višestrukih mikrotrombi u mikrovaskularnim krvnim sudovima, zatim do razvoja hipokagulacije i trombocitogeneze i razvoja hipokagulacije i razvoja zgrušavanja krvi. "potrošnja" faktora koagulacijskog sustava i povećanje funkcionalne aktivnosti antikoagulacijskog sustava i fibrinolize krvi s naknadnim iscrpljivanjem svih \\ t EX sistema.
Etiologija. Raznovrsnost i nespecifičnost DIC-a je posljedica raznolikosti uzročnih faktora njegove pojave. Tu spadaju prije svega generalizirane infekcije i septičke bolesti, sve vrste šoka, traumatska kirurgija, akušerska patologija (prijevremeno odvajanje, ručno odvajanje posteljice), akutna intravaskularna hemoliza, uremija kod zatajenja bubrega, sva terminalna stanja.
Patogeneza. Glavna karika u patogenezi generalizovane hiperkoagulacije je neravnoteža između kalikrein-kinina, koagulacije, antikoagulanta i fibrinolitičkih krvnih sistema kada veliki broj prokoagulanata i njihovih aktivatora ulaze u krvotok. To dovodi do narušavanja tako važne funkcije krvi kao očuvanja njenog normalnog agregatnog stanja, što rezultira da se u fazi hiperkoagulacije krv u krvnim sudovima koagulira i zaustavlja cirkulaciju s razvojem teških distrofičnih i funkcionalnih poremećaja u organima i tkivima koji su često nespojivi sa životom. U narednoj fazi hipokagulacije, prorjeđivanje krvi i gubitak sposobnosti zgrušavanja i agregatnih trombocita uzrokuju krvarenje, koje je slabo pogodno za terapijsku korekciju. Sa povoljnim ishodom, treći dolazi - faza oporavka, kod koje je normalizovana hemostaza.
Stanje sistema hemostaze određuje tok i ishod trudnoće za majku i fetus. U posljednjih nekoliko godina, došlo je do značajnog broja publikacija koje ukazuju na veliku ulogu trombofilnih komplikacija u uobičajenom pobačaju, smrti fetusa, abrupciji placente, u razvoju eklampsije, intrauterinog usporavanja rasta.
Glavni mehanizmi hemostaze
Sistem hemostaze ili sistem regulacije agregatnog stanja krvi (PACK) je biološki sistem koji reguliše agregaciono stanje krvi i održava hemostatski potencijal potreban organizmu. PACK sistem je mozaik, tj. hemostatski potencijal u različitim delovima protoka krvi nije isti. Ovo stanje je normalno za funkcionalni sistem. Sistem regulacije agregatnog stanja krvi uključuje:
- centralni organi sistema - koštana srž, jetra, slezina;
- periferne formacije - mastociti, endometrij i drugi slojevi vaskularnog zida, krvne ćelije;
- lokalni regulatorni sistemi - vegetativni nervni sistem, subkortikalne strukture.
Sistem hemostaze je regulisan složenim neurohumoralnim mehanizmima. Ovi mehanizmi stvaraju uslove pod kojima lokalni proces zgrušavanja, koji je neophodan za zaustavljanje krvarenja, ne ulazi u proces opšte intravaskularne koagulacije tokom normalnog funkcionisanja sistema.
Postoje četiri glavne veze u sistemu hemostaze:
- Vaskularno-trombocitna veza;
- Procoagulants;
- Fibrinolitička veza;
- Inhibitori koagulacije linkova.
Vaskularno-trombocitna veza
Vaskularno-trombocitni sistem hemostaze se često naziva primarna hemostaza. Endotel krvnih sudova igra važnu ulogu u održavanju agregatnog stanja cirkulirajuće krvi. To je zbog sljedećih značajki:
- sposobnost formiranja i oslobađanja u krvi snažnog inhibitora agregacije trombocita - prostaciklina (metabolita arahidonske kiseline);
- proizvodnju aktivatora fibrinolize tkiva;
- nemogućnost kontaktiranja aktivacije sistema zgrušavanja krvi;
- stvaranje antikoagulantnog potencijala na interfejsu krv / tkivo fiksiranjem kompleksa heparin-antitrombin III na endotelu;
- sposobnost uklanjanja aktiviranih faktora zgrušavanja iz krvotoka.
Učešće trombocita u hemostazi određeno je njihovom sposobnošću da se pridržavaju mesta oštećenja endotela, procesom njihove agregacije i formiranjem primarnog čepa trombocita, kao i njihovom sposobnošću da održavaju vaskularni spazam izlučivanjem vazoaktivnih supstanci - adrenalina, noradrenalina, serotonina, ADP-a, itd. akumuliraju i izlučuju supstance koje promovišu adheziju i agregaciju.
Stoga su brojne studije dovele do zaključka da se primarna hemostaza izvodi uglavnom trombocitima, a ne koagulacijom krvi. Vodeća uloga u primjeni primarne hemostaze pripada funkciji adhezivnog agregiranja trombocita.
Adhezija - prianjanje trombocita na mesto oštećenja zida krvnih sudova, kolagenskih vlakana vaskularnog zida, mikrofibrina i elastina. Najvažniji plazma kofaktori ovog procesa su ioni kalcijuma i villebrandov faktor sintetizovani u proteinu endotela i glikoproteinima trombocitnih membrana. Fiziološka svrha adhezije - za zatvaranje defekta u vaskularnom zidu. Istovremeno sa adhezijom nastavlja se agregacija trombocita. U isto vreme, trombociti se ne lepe zajedno, već se i drže na adheriranim pločicama, čime se formira hemostatski čep. U procesu adhezije i agregacije, trombociti iz trombocita aktivno sekvestriraju granule koje sadrže supstance koje poboljšavaju proces agregacije i formiraju njegov drugi talas. Reakcija oslobađanja faktora trombocita - ADP, adrenalin, norepinefrin, serotonin, antiheparinski faktor, beta-tromboglobulin, itd. Kasnije se izlučuju granule koje sadrže lizosomske enzime (reakcija oslobađanja II). Oslobađanje adrenalina, norepinefrina i serotonina ne samo da povećava agregaciju, već doprinosi i sekundarnom spazmu krvnih sudova, što je praćeno pouzdanim fiksiranjem čepa trombocita na mestu oštećenja posude. Kao rezultat interakcije faktora trombocita i plazme u području hemostaze, formira se trombin, koji ne samo da pojačava agregaciju trombocita, već istovremeno stimulira koagulaciju krvi, što rezultira stvaranjem fibrina krvnog ugruška koji postaje gust i nepropustan za plazmu i serum, te dolazi do povlačenja.
U velikoj mjeri, mehanizam agregacije trombocita postao je jasan nakon otkrića prostaglandina u trombocitima i vaskularnom zidu. Različiti agensi za agregaciju aktiviraju fosfolipazu A1, koja uzrokuje uklanjanje arahidonske kiseline iz fosfolipida, moćne agregatne supstance. Pod uticajem sintetaze prostaglandina nastaju ciklični endosperoksidi prostaglandina koji stimulišu kontrakciju fibrila u trombocitima i imaju snažan agregatni efekat. Pod uticajem tromboksan sintetaze, tromboksan A1 se sintetizira u trombocitima. Ovo posljednje doprinosi transportu Ca 2+ u trombocite, što dovodi do formiranja ADP - glavnog stimulatora endogenog agregiranja. Nivo univerzalnog biološkog nosača cAMP regulisan je adenilat ciklazom, katalizirajući reakciju ATP-cAMP.
Sličan proces se dešava u vaskularnom endotelu - prostaglandini endoperoksidi nastaju iz arahidonske kiseline pod uticajem sintetaze prostaglandina. Nadalje, pod uticajem prostaciklin sintetaze, formira se prostacklin (prostaglandin L), koji ima snažan dezagregirajući efekat i aktivira adenilat ciklazu.
Dakle, tzv. tromboksan - ravnoteža prostaciklina - jedan od glavnih regulatora stanja tonusa krvnih žila i agregacije trombocita.
Prokoagulant Link Hemostasis
U procesu koagulacije krvi učestvuju jedinjenja sadržana u plazmi (prokoagulanti). To je kompleksan višestupanjski enzimski proces, koji se može podijeliti u 3 faze.
- Faza I - kompleks reakcija koje dovode do formiranja protrombinskog aktivnog kompleksa ili protrombinaze. Kompleks uključuje faktor X, treći faktor trombocita (fosfolipid), ione faktora V i Ca 2+. Ovo je najteža i najduža faza.
- Faza II - pod uticajem protrombinaze protrombin prelazi u trombin.
- Faza III - pod uticajem trombina, fibrinogen prelazi u fibrin.
Ključna tačka u formiranju protrombinaze je aktiviranje faktora koagulacije X, što se može postići pomoću dva glavna mehanizma za pokretanje procesa koagulacije - spoljašnji i unutrašnji.
Sa spoljnim mehanizmom, koagulacija se stimuliše ulaskom tkiva tromboplasmina (III ili kompleksa fosfolipid-apoprotein III) u plazmu. Ovaj mehanizam određen je testom protrombinskog vremena (PT).
Sa unutrašnjim mehanizmom zgrušavanja vrši se bez učešća tkivnog tromboplastina. Pokretački faktor za ovaj put koagulacije je aktivacija faktora X. Aktivacija faktora X može nastati zbog kontakta sa kolagenom u slučaju oštećenja vaskularnog zida ili puta enzima pod uticajem kalikreina, plazmina ili drugih proteaza.
I sa spoljašnjim i unutrašnjim putem koagulacije, interakcija i aktivacija faktora se vrši na fosfolipidnim membranama, na kojima se fiksiraju faktori koagulacije proteina uz pomoć Ca jona.
Nomenklatura faktora zgrušavanja plazme:
- I - fibrinogen;
- II - protrombin;
- III - tkivni tromboplastin;
- IV - kalcijum;
- V - faktor ubrzanja;
- VI - aktivator V faktora;
- VII - prokonvertin;
- VIII - antihemofilni globulin A;
- IX - antihemofilni faktor B (Božićni faktor);
- X - protrombinaza;
- XI - prekursor plazma tromboplastina;
- XII - Hagemanov faktor;
- XIII - fibrinaza.
Spoljni i unutrašnji mehanizmi aktivacije sistema zgrušavanja krvi nisu izolovani jedan od drugog. Uključivanje "mostova" između njih služi kao dijagnostički znak pri prepoznavanju intravaskularne aktivacije sistema koagulacije. Kada se analiziraju rezultati glavnih testova koagulacije, treba uzeti u obzir sljedeće:
- Među faktorima koagulacije plazme, samo faktor VII učestvuje u mehanizmu vanjske koagulacije, a ako je manjkav, samo je protrombinsko vrijeme produljeno.
- Faktori XII, IX, XI, VIII i prekalikrein učestvuju samo u internom mehanizmu aktivacije, u vezi s kojim su manjkavi APTT i autokagulacijski test, dok protrombinsko vrijeme ostaje normalno.
- Kod nedostatka faktora X, V, II, I na kojima su zatvoreni oba mehanizma zgrušavanja, patologija se otkriva u svim navedenim testovima.
Pored spoljašnjih i unutrašnjih mehanizama hemokagulacije, postoje dodatni putevi aktivacije rezervi u organizmu, koji su uključeni na zahtev. Najvažniji put je makrofagno-monocitni mehanizam hemokagulacije. Kada se aktiviraju endotoksinima ili drugim infektivnim antigenima, te ćelije počinju da luče veću količinu tkivnog tromboplastina.
Inhibitori endogene koagulacije
Da bi se krv održavala u tečnom stanju i da bi se ograničio proces tromboze, neophodni su fiziološki antikoagulanti. Trenutno je poznato da su prirodni antikoagulanti velika grupa spojeva koji djeluju na različite faze procesa hemostaze. Štaviše, mnogi antikoagulanti istovremeno utiču na fibrinogenezu, generisanje kalikrein-kinin sistema, sistema komplementa.
Prirodni antikoagulanti se dijele na primarne, stalno prisutne u plazmi i krvnim stanicama i djeluju nezavisno od nastanka ili otapanja krvnog ugruška, a sekundarne, koje se javljaju tijekom koagulacije krvi i fibrinolize, zbog proteolitičkog djelovanja enzima na supstratu. Antitrombin III (AT III) čini do 75% prirodnog antikoagulantnog potencijala. Antitrombin III je u stanju da blokira protrombinazu i spoljašnjim i unutrašnjim mehanizmima, budući da je, kao inhibitor faktora XIIa, XIa, IXa, VIIIa, kalikreina, A III vezuje plazmin. Aktivnost antitrombina III je pojačana više od 100 puta u formiranju kompleksa sa heparinom. Heparin nije povezan sa antitrombinom III nema antikoagulantno djelovanje. Sa smanjenjem nivoa antitrombina III dolazi do teškog trombofilnog stanja koje se karakteriše rekurentnom trombozom, plućnom tromboembolijom i srčanim udarima. Kada se antitrombin III smanji ispod 30%, pacijenti umiru od tromboembolije, a heparin nema antikoagulantni efekat na njihovu krv. Nedostatak antitrombina III formira heparinsku rezistenciju.
Prirodni antikoagulansi uključuju protein C, protein S, alfa2-makroglobulin.
Protein C je proenzim, aktiviran trombinom i faktorom Xa. Aktivacija je u kombinaciji sa fosfolipidom i kalcijem. Proces je pojačan pod uticajem trombomodulina i proteina S, koji slabi sposobnost trombina da aktivira faktore VIII i V. Sa nedostatkom proteina C postoji tendencija ka trombozi, koja se primećuje kod akutnog DIC, respiratornog distres sindroma, itd.
U procesu koagulacije krvi i fibrinolize, sekundarni, prirodni antikoagulanti nastaju kao rezultat daljnje enzimske degradacije faktora koagulacije.
Patološki antikoagulansi su odsutni u krvi normalnim uslovimaali se pojavljuju sa različitim poremećajima imuniteta, uključujući antitela na faktore zgrušavanja krvi, najčešće na faktore VIII i V (često se javljaju nakon poroda i masivnih transfuzija krvi i imunih kompleksa - lupus antikoagulant, antitrombin V).
Fibrinolitički sistem
Fibrinolitički sistem se sastoji od plazminogena i njegovih aktivatora i inhibitora.
Aktivatori plazminogena su grupa faktora koji pretvaraju plazminogen u plazmin. To uključuje takve tvari kakurokinaza, bakterijski enzimi. Aktivni plazmin se brzo blokira antiplasminima i eliminiše iz krvotoka. Aktivacija fibrinolize, kao i aktivacija koagulacije krvi, vrši se i spoljašnjim i unutrašnjim stazama.
Unutrašnji put aktivacije fibrinolize određen je istim faktorima kao koagulacija krvi, tj. faktori XIIa ili XIII sa kalikreinom i kininogenom. Vanjski put aktivacije provodi se na račun aktivatora tkivnog tipa sintetiziranog u endotelu. Aktivatori tkivnog tipa nalaze se u mnogim tkivima i tjelesnim tekućinama, krvnim stanicama. Zabranjena je fibrinoliza antiplasminima alfa2-globulina, alfa2-makroglobulina, antitripsina, itd. Sistem plazmina prilagođen je fibrinskoj lizi u ugrušcima (trombi) i topljivim fibrin-monomernim kompleksima (RFMC). I tek kada se pojavi njegova prekomerna aktivacija dolazi do lize fibrina, fibrinogena i drugih proteina. Aktivni plazmin uzrokuje sekvencijalno razdvajanje fibrinogena / fibrina formiranjem njihovih proizvoda razgradnje (PDF), čije prisustvo ukazuje na aktivaciju fibrinolize.
Po pravilu, u većini kliničkih posmatranja aktivacija fibrinolize je sekundarna i povezana je sa diseminovanom intravaskularnom koagulacijom krvi.
U procesu koagulacije i fibrinolize, nastali sekundarni, prirodni antikoagulanti - PDF i drugi potrošeni faktori koagulacije - su biološki aktivni, koji djeluju kao antiplatetični agensi i antikoagulanti.
Trenutno postoje imunološke trombofilne komplikacije i nasljedni defekti hemostaze.
Sistem hemostaze tokom trudnoće
Dominantno gledište je da se u tijelu trudne žene stvaraju određeni uslovi za razvoj sindroma diseminirane intravaskularne koagulacije. To se ogleda u povećanju ukupnog koagulacijskog potencijala (ukupna aktivnost faktora koagulacije), povećanju funkcionalne aktivnosti trombocita sa određenim smanjenjem njihovog broja, smanjenjem fibrinolitičke aktivnosti sa povećanjem PDF-a, smanjenjem aktivnosti antitrombina III sa određenim smanjenjem sadržaja. Ove osobine su kompenzatorne i adaptivne prirode i neophodne su kako za normalno formiranje placentarnog kompleksa tako i za ograničavanje gubitka krvi tijekom poroda. U aktiviranju sistema hemostaze važnu ulogu imaju promjene u ukupnoj hemodinamici u tijelu trudnice. Za normalno funkcionisanje placentnog sistema u uslovima visokog koagulacijskog potencijala krvi, stupaju na snagu kompenzatorno-adaptivni mehanizmi: povećanje broja terminalnih resica malog kalibra sa hiperplazijom i perifernim rasporedom kapilara, smanjenje debljine placentarne barijere sa stanjivanjem sincitiuma, formiranje sincytiocapillary membrana, sincitium zglobova.
Karakteristike funkcionisanja sistema hemostaze povezane su sa izvesnim promenama u sistemu spiralnih arterija materice. To su invazija trofoblast ćelija u zid spiralnih arterija, zamjena unutrašnje elastične membrane i unutrašnjeg medija debelim slojem fibrina, narušavanje integriteta endotela i izlaganje kolendnih subendotelnih struktura. U tom procesu je važan i razvoj intervilnog prostora sa svojim svojstvenim morfološkim i hemodinamskim osobinama.
Karakteristike sistema hemostaze tokom fiziološke trudnoće određuju se formiranjem uteroplacentalne cirkulacije.
Nivo trombocita sa nekomplikovanom trudnoćom ostaje gotovo nepromenjen, iako postoje studije u kojima se smanjuje nivo trombocita. Sa smanjenjem nivoa trombocita ispod 150000 / ml, potrebno je istraživanje kako bi se utvrdili uzroci trombocitopenije.
Tokom trudnoće, uočava se povećanje koagulantnog potencijala, organizam se priprema za moguće krvarenje tokom porođaja. Uočen je porast svih faktora koagulacije uz izuzetak faktora XI i XIII.
Povećanje nivoa fibrinogena počinje od trećeg meseca trudnoće i, uprkos povećanju obima plazme u cirkulaciji, nivo fibrinogena na kraju trudnoće raste najmanje dva puta u odnosu na stanje koje nije trudno.
Aktivnost faktora VIII (von Willebrandov faktor) takođe se povećava ne samo kod zdravih žena, već i kod pacijenata - provodnika hemofilije i pacijenata sa von Willebrandovom bolešću. Treba imati na umu da kod blagih i umjerenih stupnjeva ove bolesti, nivo ovog faktora može biti gotovo normalan. Za razliku od opšteg porasta faktora zgrušavanja, blagi pad faktora XI na kraju trudnoće i izraženiji pad faktora XIII (faktor stabilizacije fibrina) zabeleženi su tokom trudnoće. Fiziološka uloga ovih promjena još nije jasna.
Potencijal koagulacije krvi se povećava čak i kada se smanjuje nivo antitrombina III, protein C raste uglavnom u postpartalnom periodu, a protein S se smanjuje tokom trudnoće i značajno se smanjuje nakon poroda.
Tokom trudnoće došlo je do smanjenja fibrinolize na kraju trudnoće i tokom poroda. U ranom postpartalnom periodu, aktivnost fibrinolize se vraća u normalu. Postoje kontradiktorni podaci o prisustvu FDP u krvotoku. Prema studiji, došlo je do blagog povećanja FDP-a u posljednjim mjesecima trudnoće. Prema istraživanju, sa nekompliciranim tokom trudnoće, povećanje sadržaja proizvoda razgradnje nije otkriveno do početka rada. Prema J. Rand et al. (1991), nivo nekih fragmenata proizvoda degradacije fibrina raste od 16 nedelja gestacije i doseže plato za 36-40 nedelja. Međutim, značajno povećanje PDF-a tokom trudnoće je vjerovatno odraz fibrinolitičkog procesa uslijed aktivacije intravaskularne koagulacije.
Promene u sistemu hemostaze kod trudnica sa antifosfolipidnim sindromom
Parametri hemostatskog sistema kod trudnica sa antifosfolipidnim sindromom značajno se razlikuju od onih kod žena sa fiziološkom trudnoćom. Od početka trudnoće, većina pacijenata ima promene u hemostazi trombocita. Agregacija trombocita tokom stimulacije ADP-a je 55-33% viša nego tokom fiziološke trudnoće. Tendencija povećanja agregacije ostaje u pozadini antitrombocitne terapije.
Agregacija trombocita pod dejstvom kolagena je 1,8 puta veća nego kod fiziološkog toka trudnoće. Agregacija trombocita adrenalinom je 39% viša nego u kontrolnoj grupi. Ako pod uticajem terapije nije moguće smanjiti ove pokazatelje, onda je takva perzistentna hiperaktivnost trombocita osnova za povećanje doze antitrombocitnih agenasa ili propisivanje dodatnih antiplatketnih agenasa. Indikatori ristomicina - agregacije u prosjeku u prvom tromjesečju ostaju u granicama normale. Istraživanja su pokazala da od rane trudnoće kod pacijenata sa APS postoji pojačana reakcija trombocita na efekte bioloških induktora, identifikovanih uglavnom u testovima funkcionalne aktivnosti trombocita, kao što je agregacija pod uticajem ADP 1x10 3 M i 1x10 5 M, arahidonska kiselina.
Prilikom ocjenjivanja karakteristika kvaliteta po tipovima agregatograma, nije uočena disagregacija (reverzibilna agregacija) u svim slučajevima kada je izložen čak i slabim stimulusima ADP 1 x 10 7 M. Na to ukazuje promjena profila krivulja prema takozvanim "atipičnim" hiperfunkcionalnim agregatogramima.
Indikatori plazma hemostaze u prvom trimestru trudnoće su takođe promenjeni u odnosu na kontrolu: zapaženo je značajno ubrzanje AVR, indikator r + k je skraćen na tromboelastogramu, indeks strukturnih svojstava fibrinskog ugruška - ITP bio je značajno veći.
Tako, u trudnica sa APS-om, u prvom trimestru uočava se umjerena hiperkoagulacija u plazmi poveznice hemostaze, koja se razvija ranije od hiperkoagulacije povezane s adaptacijom hemostaze tijekom fiziološki napredne trudnoće. Ove promene koje određuju hiperaktivnost hemostaze uopšte u prvom trimestru trudnoće ne smatraju se patološkom aktivacijom stvaranja intravaskularnog tromba, jer izuzetno rijetko u ovoj gestacijskoj dobi uočili smo pojavu markera DIC - produkata degradacije fibrina i fibrinogena (FDP). Sadržaj PDF-a u prvom tromjesečju nije prelazio 2x10 g / l. To je bila osnova za sagledavanje hiperaktivnosti trombocita i hemostaze plazme kao hiperkoagulacije koja ne odgovara gestacijskoj starosti i pozadini za razvoj DIC.
U drugom tromjesečju trudnoće, uprkos terapiji, uočene su promjene u hemostaznoj vezi plazme. Otkriveno je da je APTTV 10%, a AVR 5% kraći nego tokom fiziološke trudnoće. Ovi podaci ukazuju na povećanu hiperkoagulaciju. Isti trend je uočen u trombotičkom elastogramu: stope r + k hronometrijske koagulacije, Ma parametri i ITP su veći nego u toku fiziološke trudnoće.
Kod hemostaze trombocita uočava se statistički značajno povećanje agregacije i povećanje hiperfunkcionalnih tipova krivulja pri izlaganju slabim stimulansima, što ukazuje na postojanu hiperaktivnost trombocita kod trudnica sa APS rezistentnom na terapiju.
U trećem trimestru trudnoće uočena je ista tendencija povećanja fenomena hiperkoagulacije, uprkos tekućoj terapiji. Pokazatelji koncentracije fibrinogena, AVR i APTT ukazuju na razvoj hiperkoagulacije. Iako zbog velike kontrole hemostaziograma, terapijske mjere mogu zadržati hiperkoagulaciju u granicama blizu fizioloških parametara.
S obzirom da se glavni, prirodni inhibitori koagulacije krvi sintetiziraju vaskularnim zidom, uključujući placentalne žile, od velikog je interesa procijeniti ukupnu aktivnost inhibitora aktivatora plazminogena (PAI) kako trudnoća napreduje kod žena s antifosfolipidnim sindromom. U dinamici određivanja trudnoće sadržaj PAI pokazao je da kod trudnica sa antifosfolipidnim sindromom ne dolazi do povećanja blokiranja PAI 1 i placentnog PAI 2.
Maksimalno povećanje inhibitora aktivatora plazminogena u pojedinačnim opažanjima bilo je 9,2–9,7 U / ml (normalno, ovaj indikator je 0,3–3,5 U / ml) u odnosu na prilično visoku aktivnost i sadržaj plazminogena - glavnog fibrinolitičkog supstrata (112). -115% i 15,3-16,3 g / l, sa normom od 75-150% i 8 g / l, respektivno. Rani znaci patološke aktivnosti hemostatskog sistema (trombinemija) u prvom trimestru u odnosu na nivo neaktivnog antitrombina III kompleksa (TAT) uočeni su samo u pojedinačnim slučajevima, što potvrđuje stvarnu intravaskularnu generaciju prokoagulantne aktivnosti.
Studije komponenti antikoagulantnih mehanizama sistema hemostaze omogućile su da se utvrdi velika varijabilnost u sadržaju proteina C (PrS), u većini slučajeva smanjenje nivoa ne zavisi od trajanja trudnoće. Maksimalna aktivnost ProS ne prelazi 97%, u većini posmatranja - 53-78% (norma je 70-140%).
Individualna analiza sadržaja inhibitora aktivatora plazminogena u drugom tromjesečju trudnoće pokazala je oštar porast inhibitora aktivatora plazminogena na 75 U / ml u samo 1 slučaju, dok je postojala kombinacija porasta inhibitora plazminogen aktivatora sa teškom patologijom AT III, aktivnost 45,5%, koncentracija 0,423 g / l. U svim drugim slučajevima, sadržaj inhibitora aktivatora plazminogena kretao se u rasponu od 0.6–12.7 U / ml, u prosjeku 4.7 ± 0.08 U / ml. Nadalje, u trećem tromjesečju, sadržaj inhibitora aktivatora plazminogena je također ostao nizak, fluktuacije u rasponu od 0,8 do 10,7 U / ml, u prosjeku 3,2 ± 0,04 U / ml, samo u jednom opažanju - 16,6 U / ml. S obzirom da obično nagli porast sadržaja inhibitora aktivatora plazminogena doprinosi smanjenju fibrinolitičke aktivnosti i lokalnom stvaranju tromba (zbog supresije reparativne fibrinolize), činjenice koje smo primijetili mogu se posmatrati kao nedostatak endotelnog odgovora kod trudnica sa APS, koji se sintetizira endotelijalni vaskularni endotel zidovi, i, što je još važnije, odsustvo sistema placentne komponente PAI 2, koje proizvode placentalne žile. Moguće objašnjenje faktora koje smo primetili može biti narušena funkcija endotelnih ćelija i, pre svega, placentnih krvnih sudova kod trudnica sa antifosfolipidnim sindromom, verovatno zbog fiksacije kompleksa antigen-antitelo na endotelu.
Važno je napomenuti da je značajno smanjenje aktivnosti Proc u drugom tromjesečju trudnoće 29% niže nego u kontrolnoj grupi.
Vrednovanje fibrinolitičkog sistema pokazalo je sledeće rezultate: u većini posmatranja plazminogenska aktivnost bila je visoka u prvom trimestru 102 ± 6,4%, a koncentracija 15,7 ± 0,0 Eg / l; u drugom tromjesečju aktivnost plazminogena bila je podložna još većim fluktuacijama od 112 do 277% i koncentraciji od 11,7 g / l do 25,3 g / l, u prosjeku 136,8 + 11,2%, koncentracija 14,5 + 0,11 g / l. U trećem tromjesečju ostala su slična stanja: aktivnost plazminogena kretala se od 104 do 234% (norma je bila 126,8 ± 9,9%), koncentracija je bila od 10,8 do 16,3 g / l, u prosjeku 14,5 + 0,11 g / l. . Dakle, fibrinolitički potencijal kod trudnica sa antifosfolipidnim sindromom je prilično visok.
Nasuprot tome, sadržaj glavnog inhibitora fibrinolize alfa2-makroglobulina (alfa 2Md) bio je prilično visok u prvom tromjesečju trudnoće, u rasponu od 3,2 do 6,2 g / l (obično 2,4 g / l), u prosjeku 3,36 ± 0,08 g / l; u II trimestru, odnosno 2,9 do 6,2 g / l, u prosjeku 3,82 ± 0,14 g / l.
Slični podaci su dobijeni u pogledu sadržaja alfa1-antitripsina (alfa-ALAT), koji se u svim trimestrima trudnoće kretao od 2,0 do 7,9 g / l. Pošto su CL-Mg i a1-AT puferi inhibitora odloženih i indirektnih efekata, njihov efekat na aktivaciju fibrinolitičkog sistema, čak iu uslovima visokog nivoa plazminogena, ispoljio je smanjenje fibrinolitičkog potencijala kod trudnica sa antifosfolipidnim sindromom, slično kao u fiziološkom toku trudnoće.
Navedene karakteristike hemostaznog sistema naglašavaju veliki značaj kontrolnih studija hemostaze tokom trudnoće za optimizaciju antitrombotske terapije i prevenciju jatrogenih komplikacija.
Proučavanje hemostatskog sistema prije porođaja pokazalo je da hemostatski potencijal ostaje netaknut, i uprkos antiplatetičkoj terapiji, postoji tendencija hiperfunkcije trombocita.
Imajući u vidu da pacijenti sa antifosfolipidnim sindromom tokom trudnoće primaju antitrombotske agense, a nakon porođaja postoji visok rizik od tromboembolijskih komplikacija svojstvenih pacijentima sa antifosfolipidnim sindromom, izučavanje hemostaze u postporođajnom periodu je izuzetno važno.
Podcjenjivanje hemostaziograma, prestanak terapije odmah nakon poroda može dovesti do ubrzanog razvoja hiperkoagulacije i tromboembolijskih komplikacija. Istraživanja su pokazala da potencijal za zgrušavanje krvi ostaje visok nakon porođaja, čak iu slučajevima kada su pacijenti primali terapiju heparinom. Studije sistema hemostaze treba sprovesti 1, 3 i 5 dana nakon rođenja. Umerena hiperkoagulacija je zabeležena kod 49% puerpera, au 51% puerpera je zabeležena aktivacija hemostaznog sistema - povećanje hiperkoagulacije i pojavljivanje PDF-a.
Kongenitalni defekti hemostaze
Trenutno se velika pažnja posvećuje genetski određenim oblicima trombofilije, koja je, kao i antifosfolipidni sindrom, praćena tromboembolijskim komplikacijama tokom trudnoće i dovodi do gubitka trudnoće u bilo kojoj fazi. Glavni uzroci nasljedne trombofilije: nedostatak antitrombina, proteina C i S, heparin-kofaktor H, nedostatak faktora XII, dis- i hipoplazminogenemija, disfibrinogenemija, nedostatak tkivnog aktivatora plazminogena, Leiden-ova mutacija faktora koagulacije gena V.
Pored ovih poremećaja, nasledna trombofilna stanja poslednjih godina uključuju hiperhomocisteinemiju, stanje u kome, zbog naslednog defekta enzima, metilenetetrahidrofolat reduktaze, postoji rizik od razvoja venske i arterijske tromboze, a time i gubitka trudnoće sa mogućim ranim razvojem eklampsije. Treba napomenuti da je u jednoj od najnovijih publikacija konstatovano da je hiperhomocisteinemija detektovana u 11% populacije Evropljana. Za razliku od drugih nasljednih hemostaznih defekata, ova patologija pokazuje rane gubitke trudnoće već u prvom tromjesečju. Za hiperhomocisteinemiju, folna kiselina je veoma efikasna prevencija tromboze.
Prilikom identifikacije trudnica sa naslednom trombofilijom neophodna je veoma pažljiva procena podataka iz porodične istorije. Ako imate istoriju neposrednih srodnika tromboembolijskih komplikacija u ranom uzrastu, tokom trudnoće, ako koristite hormonsku terapiju, uključujući oralne kontraceptive, trebate biti pregledani u vezi sa hereditaznim defektima, kod kojih je rizik od tromboembolijskih komplikacija izuzetno visok.
Antitrombin inaktivira trombin, faktore IXa, Xa, XIa i CPA. Nedostatak alfa1-antitrombina je visoko trombogenetski i daje do 50% slučajeva tromboze tokom trudnoće. Zbog heterogenosti povreda, učestalost pojavljivanja ovog defekta varira od 1: 600 do 1: 5000.
Protein C inaktivira faktore Va i VIIIa. Protein S djeluje kao kofaktor proteina C, pojačavajući njegovo djelovanje. Nedostatak proteina C i S javlja se sa frekvencijom od 1: 500. Protein C je praktično nepromenjen tokom trudnoće, protein S se smanjuje u drugoj polovini trudnoće i vraća se u normalu ubrzo nakon porođaja. Stoga, ako se određivanje proteina S vrši tokom trudnoće, mogu se dobiti lažno pozitivni rezultati.
Poslednjih godina, mnoge publikacije o trombofiliji zbog mutacija gena V faktora, to je takozvana Leiden-ova mutacija. Kao rezultat ove mutacije, protein C ne utiče na faktor V, što dovodi do trombofilije. Ova patologija je pronađena 9% evropske populacije. Ova mutacija mora biti potvrđena DNK testom za faktor V Leiden. Učestalost pojave Leidenove mutacije značajno varira. Tako je, prema švedskim istraživačima, učestalost ovog defekta hemostaze kod trudnica sa trombozom iznosila od 46 do 60%, dok je u Engleskoj iznosila samo 14%, au Škotskoj 8%.

PATOFIZIOLOGIJA HEMOSTAZNOG SISTEMA
Vrednost hemostatskog sistema
1. Očuvanje krvi u tekućem stanju (adekvatan odnos aktivnosti koagulacionog i antikoagulacijskog sistema) \\ t
2. Sprečavanje i zaustavljanje krvarenja (održavanje konstantnog volumena krvi u cirkulaciji)

VRSTE HEMOSTAZA
Vaskularno-trombocit
(PRIMARY)
- ZAUSTAVLJANJE KRVENJA U MIKRO BRODOVIMA
COAGULATION
(SEKUNDARNO)
FORMIRANJE FIBRINA

KOMPONENTE SISTEMA HEMOSTAZA
* VASKULARNI ZID
* THROMBOCYTES (monociti, eritrociti)
* PLASMA SYSTEMS:
- PROKOAGULYANTY
- ANTICOAGULANTS
- FIBRINOLYTIC
- KALLIKREIN-KININOVAYA

KLASIFIKACIJA POREMEĆAJA HEMOSTAZE
ZA ETIOLOGIJU
- HEREDITAR
- PRISTUPNA
ZA MEHANIZAM RAZVOJA
- VASKULARNI POREMEĆAJI
HEMOSTASIS
- POREMEĆAJI KOAGULATORNE HEMOSTASE
ZA UPRAVLJANJE PROMJENAMA
- HIPOKOAGULACIJA
- Hiperkoagulacija

HIPOKOAGULACIJA
Smanjena sposobnost krvnog ugruška sa tendencijom ponovnog krvarenja i krvarenja (spontano ili nakon lakših povreda)

ETIOLOGIJA
1. THROMBOCYTOPIA
2. trombocitopatije
3. VASOPATHY
4. COAGULOPATHY

Trombocitopenija
Patološko stanje karakterizirano smanjenjem broja trombocita u krvi. (manje od 150 · 109 / l)

HEREDITARNA THROMBOCYTOPENIA
Po pravilu, to je istovremeno praćeno abnormalnim defektima trombocita

PRIDRUŽENA TROMBOCITOPENIJA (KLASIFIKACIJA POD RAZVOJNIM MEHANIZMOM)
ŠTETE PLATELETA
- imuni kompleksi
- mehanička trauma (splenomegalija, hemangioma)
OBRAZOVANJE TROMBOCITOM
(aplastična anemija, hemijsko i zračenje oštećenja crvene koštane srži, zamjena hematopoetskog tkiva tumorom)
POVEĆANA UPOTREBA PLATELETA
(tromboza, DIC)

Imunska trombocitopenija
Heteroimmune
* Pojavljuje se češće u djeca
** Razlog - promjene u antigenskoj strukturi trombocita (tijekom slijeganja rubeole, velikih boginja, adenovirusnih virusa; haptena dobivenih lijekovima - kinidina, sulfonamida, rifampicina; vakcina)
***Povoljan kurs (ako je uzrok eliminiran, dolazi do potpunog oporavka)

Imunska trombocitopenija
AUTO-IMUN
Pojavljuje se češće u odrasli
Razlog - nedostatak imunološke tolerancije na antigene vlastitih trombocita
Provokativni faktori: lekove, viruse, bakterije

Autoimuna trombocitopenija
VERLEHOPH DISEASE
(autoimuna kronična trombocitopenična purpura)
* Na površini trombocita Ig G povećava se 10 puta
Glavno mjesto sinteze Ig G je slezena
* Princip tretmana:
- splenektomija
- kortikosteroidi
- imunosupresivi
* Ne postoji potpuni lijek.

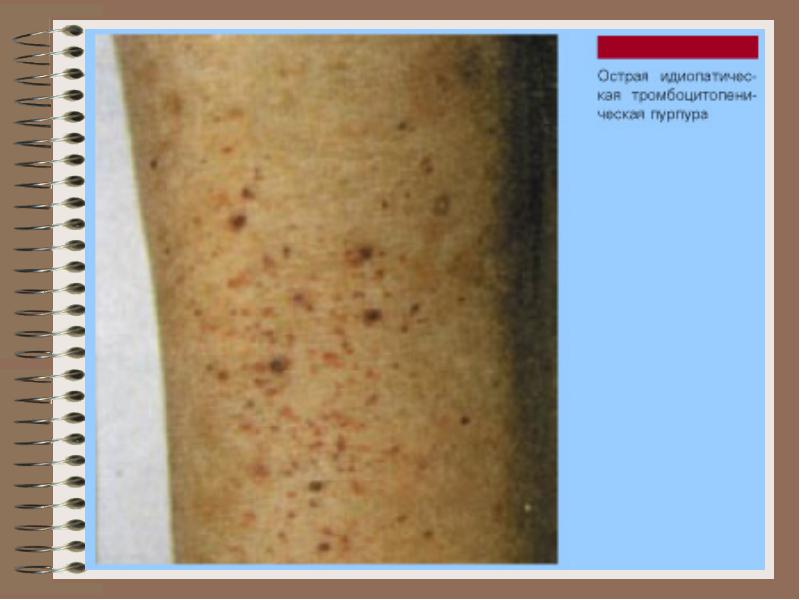
Trombocitopatije
Abnormalna hemostaza zbog kvalitativne inferiornosti ili disfunkcije trombocita, koju karakteriše kršenje vaskularne trombocitne hemostaze, pojava krvarenja tkiva i organa

BEZ KRŠENJA REAKCIJE OSLOBOĐENJA GRANULOVA
Glantsman Thrombasthenia
* Nasleđivanje - autosomno recesivno
*Razlog - odsustvo glikoproteina 2b i 3a u ljusci trombocita
*Patogeneza- trombociti ne interaguju sa fibrinogenom i ne agregiraju se
*Znakovi: petehije, krvarenje iz nosa, krvarenje iz maternice ( može biti smrtonosno !!)

Nasledna trombocitopatija
S POVREDOM REAKCIJE OTPUŠTANJA GRANULOVA
Nasljeđivanje - autosomno recesivno
Razlog - oslabljena aktivnost cikloksigenaze, niska aktivnost kontraktilnih proteina
Patogeneza - nedostatak agregacije u interakciji sa kolagenom, nedostatak oslobađanja granula
Znakovi:

Nasledna trombocitopatija
SA KRŠENJANJEM I OSLOBAĐANJEM SADRŽAJA GRANULI
Bolest Herjman Pudlak (AR)
* Razlog - kršenje nakupljanja gustih granula (ADP, adrenalin, serotonin, Ca2 +)
* Patogeneza - ne postoji agregacija u interakciji sa kolagenom, ne dolazi do oslobađanja sadržaja granula
* Znakovi: petehije, krvarenje iz nosa, krvarenje iz materice

Nasledna trombocitopatija
S POREMEĆANJEM ADHEZIJE I AGREGACIJOM PLATELETA
Von Willebrand-Jurgensov sindrom (AR) \\ t
Razlog - Willebrandov nedostatak faktora
Patogeneza - Adhezija trombocita je smanjena zbog nedostatka faktora 8
Bernard Sul bolesti (AR) \\ t
Razlog - nedostatak glikoproteina 1 na trombocitima
Patogeneza - interakcija trombocita sa von Willebrandovim faktorom, f. 5, f. 11
Signs of - kapilarno krvarenje ( posebno opasna za vrijeme puberteta ili poroda)

Nasledna trombocitopatija
NEDOSTATAK I SMANJENA DOSTUPNOST f.3
Trombocitopatija Bowe i Ovan
Razlog - nedostatak f.3 trombocita
Patogeneza - nema interakcije trombocita i prokoagulanata
Znakovi: petehije, krvarenje iz nosa, krvarenje iz materice

Nasledna trombocitopatija
Trombocitopatija u kombinaciji sa drugim nasljednim anomalijama
Whiskott-Aldridgeov sindrom
- Razlog - u trombocitima ima nekoliko gustih granula (ADP, serotonin, adrenalin, Ca2 +), alfa granule (beta-tromboglobulin, fibrinogen, fibronektin, faktor rasta)
- Patogeneza - Smanjena adhezija i agregacija trombocita, poremećeno oslobađanje granula
- Znakovi:hemoragijski sindrom se javlja rano, može doći do fatalnog krvarenja

Stečena trombocitopatija (etiologija)
1. Leukemija- nekoliko granula u trombocitima zbog ubrzanog sazrijevanja, smanjene adhezije i agregacije
2. Pile upIg M - oštećenje receptora imunim kompleksima, narušavanje interakcije trombocita s prokoagulantima (imunološke bolesti)
3. Hipovitaminoza B12 - isprekidano oslobađanje granula
4. Efekti lijekova

Trombocitopatija
* And inhibitori sinteze tromboksana A2
steroidni antiinflamatorni lijekovi
- nesteroidni antiinflamatorni lijekovi (aspirin blokira agregaciju trombocita za 4-6 dana)
* Obrazovni stimulatori cAMP
papaverin
- eufilin
-anabolički steroidi
* Antagonisti iona Ca
verapamil
Corinthar

VASOPATHY
Hemoragijska dijateza usled funkcionalne i morfološke inferiornosti vaskularnog zida
- kongenitalne
- stečena

HORN VASOPATHY
Bol Randyu-Osler (hemoragična telangiektazija)
Bol Fabry (difuzni angioker-toma trupa)
Nasledna trombocitopenična mikroangiomatoza

HORN VASOPATHY
Razlog - nasljedni poremećaj razvoja vezivnog tkiva, uklj. vaskularni subendotel
Karakteristično
- fokalno vaskularno stanjivanje
- širenje lumena mikroviselja
- malo kolagenskih vlakana u subendotelu
- posude se lako povređuju
- slaba adhezija i agregacija trombocita zbog nedostatka kolagenih vlakana
**Signs of - krvarenje iz nosa, pluća i bronhija i gastrointestinalnog trakta (ima fatalnih ishoda)

PRIDRUŽENA VASOPATIJA
1. I diopatski (Kaposijev sarkom)
- etiologija - nepoznata
2. Stagnant (dermatitis Klotza, dermatitis Favra Rakusho)
- etiologija - hronična srčana insuficijencija, lokalna venska insuficijencija
3. Dystrophic
Purpura steroida - hiperfunkcija nadbubrežne žlijezde, liječenje kortikosteroidima - inhibiraju sintezu kolagena
Vruće - Vit.S nedostatak
Bol.Shenlein-Genokha - vaskularno oštećenje imunih kompleksa
4. Neurogenic
Klinički znaci - kožni oblici krvarenja

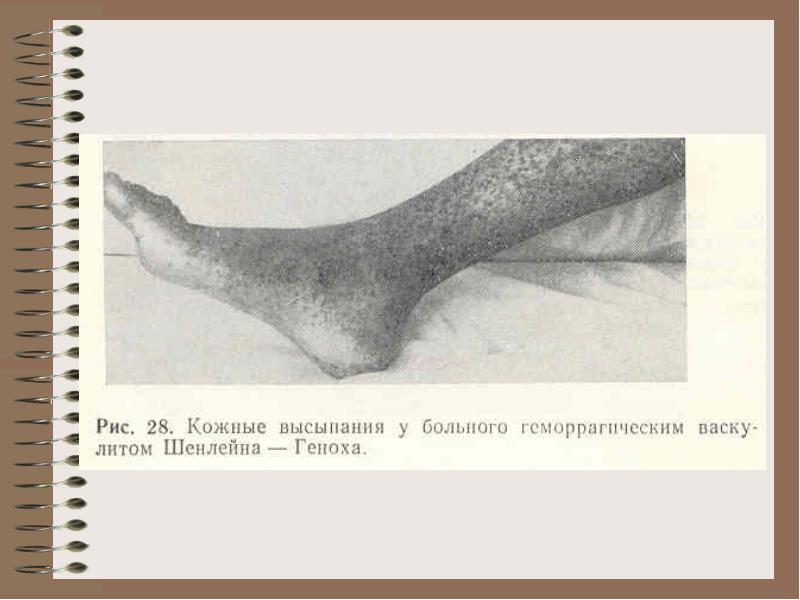
COAGULOPATHY
Hemoragijska dijateza, koja se javlja kao rezultat patologije sistema koagulacije hemostaze
** nasljedni
** stečeno

Nasledna koagulopatija
Genetski izazvan poremećaj koagulacije zbog nedostatka ili molekularne abnormalnosti supstanci odgovornih za koagulacijsku hemostazu

Nasledna koagulopatija
KLASIFIKACIJA
1. Koagulopatija zbog izolovanog kršenja unutrašnjeg mehanizma nastanka protrombinazne aktivnosti (hemofilija A, B, C, Willebrand b., Hagemanov nedostatak) \\ t
2. Koagulopatija zbog izolovanog kršenja spoljašnjeg mehanizma formiranja protrombinazne aktivnosti (hipoprokonvertinemija - nedostatak od 7 l.) \\ T
3. Kombinovano kršenje spoljašnjeg i unutrašnjeg mehanizma formiranja protrombinazne aktivnosti (parahemofilija - nedostatak od 5 lb, b. Steuart-Prouer - nedostatak od 10 lb.)
4. Kršenje završne faze koagulacije krvi (afibrinogenemija)

STATISTIKA
Među svim oblicima koagulopatije, pate:
Hemofilija A 68 - 78%
B . Willebrand 9 - 18%
Hemofilija B 6 - 13%
Hemofilija C, parahemofilija i hipoprokonvertinemija 1 - 2%
Preostali oblici - klinička kazuistika

Hemofilija A
Hemoragijska dijateza usled naslednog nedostatka prokoagulantnog dela faktora 8
Faktor 8 (protein visoke molekulske mase)
1. Glikoproteinski prokoagulant (VIII: K)
2. Glikoprotein koji vrši adheziju trombocita (VIII: FV)
3. Glikoprotein koji aktivira adheziju trombocita pod uticajem ristomicina (VIII: Rkoff)
4. Antigenski marker VIII: K (VIII: K AG)
5. Antigenski marker VIII: Rkof (VIII: Rkof AG)
Aktivnost VIII: K i VIII: PV se smanjuje sa smanjenjem multimerne strukture i samo 8 faktora

Hemofilija A
* Uh tiology - abnormalnost gena u X hromozomu, koji kontrolira sintezu prokoagulantni dio f. 8 (Viii: k)
** Ill - men (46, XhY)
** Views
- Sintetiše se hemofilija A + (antigen-pozitivna forma - anomalna) VIII: K), 8-10% pati
- Hemofilija A- (antigen-negativni oblik - nije sintetiziran) VIII: K), 90-92% pati
**** Klinika: hemoragije u velikim zglobovima, hematomi (potkožno, intramuskularno), teška i dugotrajna posttraumatska krvarenja. Moguće krvarenje u abdominalnim organima, gastrointestinalno krvarenje

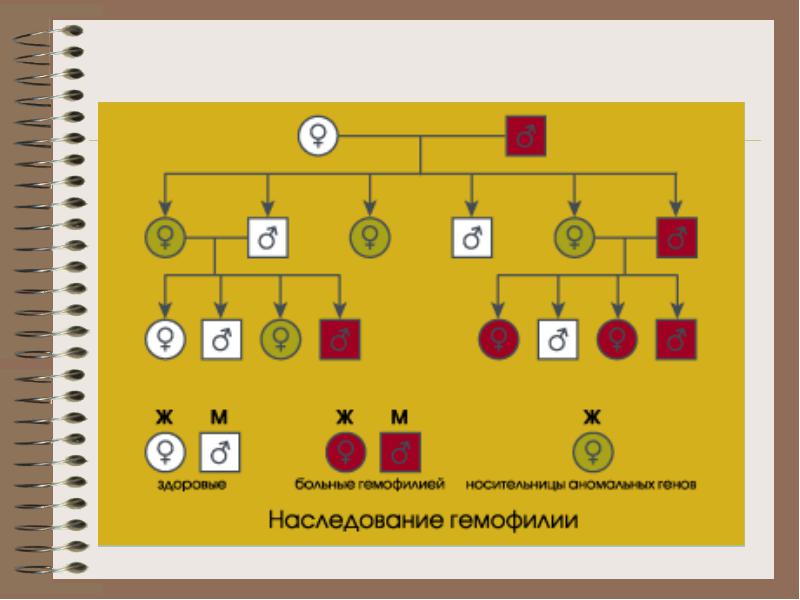
Hemofilija
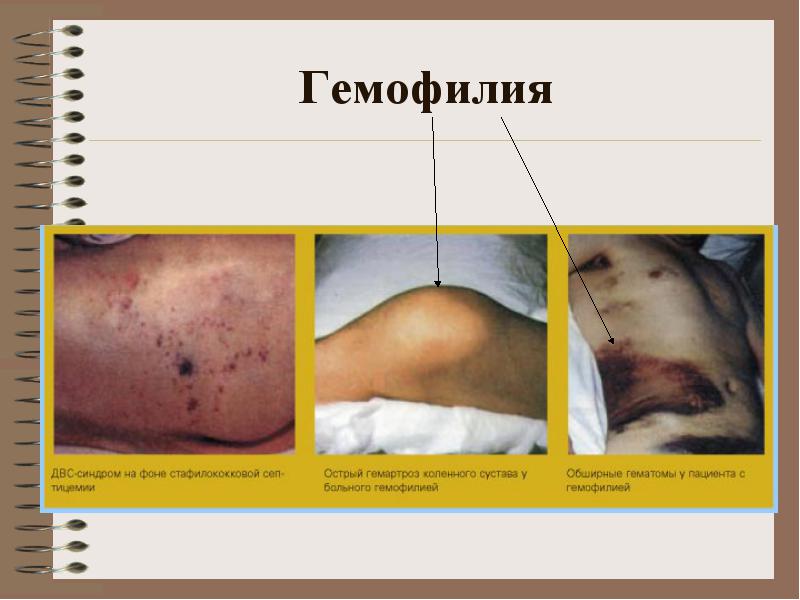
Hemofilija
Hemofilija B
Etiologija - anomalija gena u X hromozomu koja kontrolira sintezu f. 9
Sick - Men (46, XYY) \\ t
- žene (46, XhXh), (45, Xh O)
*** Pogledi
- Sintetiše se hemofilija B + (antigen-pozitivna forma - anomalna) f. 9)
- Hemofilija B- (antigen-negativni oblik - nije sintetiziran) f. 9)
Klinika: hemoragije u velikim zglobovima, hematomi (potkožno, intramuskularno), teška i dugotrajna posttraumatska krvarenja. Moguće krvarenje u abdominalnim organima, gastrointestinalno krvarenje

PRIDRUŽENA KOGULOPATIJA
Feature - polideficijentan
Etiologija
1. Imunološka inhibicija prokoagulanata (rezus konflikt) \\ t
2. Nedostatak vit. K-zavisni faktori koagulacije (7, 10, 9, 2)
a) oslabljena sinteza u crevima (disbakterioza, dijareja)
b) kršenje apsorpcije vit. K (nedostatak žuči)
c) ozbiljno oštećenje jetre
3. Predoziranje heparinom

HYPERCOAGULATION
POVEĆANI KAPACITET KRVNIH PROIZVODA U PLOVILIMA
Tromboza
DVS-SINDROM

DIC-SINDROM (SINDROM DEKOMINIRANE INTRA-VASKULARNE KRVNE KOAGULACIJE)
KLASIFIKACIJA
* Prema kliničkom toku
1) akutni (instant oblici se odlikuju teškim tokom)
2) hronična
* Po prevalenciji
1) lokalizovan
2) generalizovano

ETIOLOGIJA
Infekcije, septički uslovi
Šok (sa septičkom stopom smrtnosti od 100%)
Hirurške intervencije, opekotine
Sva terminalna stanja, srčani zastoj
Akutna intravaskularna hemoliza
Opstetrijska patologija (20-25%)
Hemoblastoza (sa o. Leukemijom - 33-45%)
Destruktivni procesi u parenhimnim organima
Alergijske reakcije

Faze DIC-a
1) Hiperkoagulacija (formiranje višestrukih krvnih ugrušaka zbog aktivacije sistema koagulacije)
2) Potrošnja koagulopatija (iscrpljivanje koagulantnog sistema, prekomjerna upotreba trombocita za formiranje krvnih ugrušaka)
3) Hipokagulacija (smanjenje aktivnosti koagulanata, aktivacija antikoagulansa, aktivacija fibrinolize)
4) Završetak (oporavak, komplikacije, smrt)

Patogeneza DIC
1) Hyperthrombinemia (tromboplastin ulazi u krv u velikim količinama iz oštećenih tkiva i potiče stvaranje trombina). Kod infekcija, aktivirani monociti makrofagi sintetiziraju vlastite koagulante (f.7, f.10, f.9, f.2)

Patogeneza DIC
2) Masivna agregacija trombocita (uzrokuje nastanak trombocitopenije nii i komplikuje krvarenje)
3) Trauma i hemoliza eritrocita (ovo proizvodi mnogo ADP, što povećava adheziju i agregaciju trombocita)

Patogeneza DIC
4) "Eksplozija humoralne proteaze" (kod aktiviranja prokoagulanata, antikoagulanata, fibrinolitika, proteina kalikrein-kinin sistema, sistem komplementa u krvi akumulira mnoge proizvode raspadanja proteina, koji su vrlo toksični i oštećuju krvne sudove i tkiva)

Patogeneza DIC
5) Iscrpljivanje fibrino-lizing sistema
(doprinosi trombozi)
6) Iscrpljivanje faktora zgrušavanja krvi
(uzrokuje razvoj krvarenja)

Klinika DIC
1. Hemokagulacijski šok
razlog
* povrede mikrocirkulacije (uzrok razvoja hipoksije tkiva)
* akumulacija toksičnih produkata proteolize
manifestacije
* snižavanje krvnog pritiska
- snižavanje centralnog venskog pritiska
krvarenje (izaziva hemoragični šok)

Klinika DIC
2. Hemostatični poremećaji
a) hiperkoagulacija
Glavna manifestacija je tromboza.
Krv koagulira in vitro
b) hipokoagulacija
Glavna manifestacija je krvarenje
(istovremeno je sistem fibrinolize osiromašen)

Klinika DIC
3. Trombocitopenija
Nastaje zbog formiranja velikog broja krvnih ugrušaka u krvnim sudovima (potrošnja trombocitopenije)

Djevojčica je nakon bolova u grlu razvila petehijski osip na koži ekstremiteta i tijela. Objektivno: broj trombocita je 80 g / l, anti-trombocitna antitela. Alergijske reakcije koje vrste (prema Coombsu i Jelli) su osnova ove bolesti?
Tip II (humoralna citotoksična)
Tip I (anafilaktički)
Tip III (imunokompleks)
Tip V (stimulirajući)
Pacijentova adhezija trombocita na kolagen je smanjena, a krvarenje iz malih žila je uočeno. Kršenje čije se veze hemostaza može tolerisati kod pacijenta?
@Vascular trombociti
Koagulacija i faza
Faza koagulacije III
Fibrinolysis
Koagulacija, II faza
Pacijentu se dijagnosticira trombocitopenija. Koje su kliničke manifestacije tipične za poremećaje hemostaze trombocita?
@ Petechia, ekhimoza (modrice)
Hemartroza
Hematomas
Smanjeno vreme krvarenja
Povećano vreme zgrušavanja krvi
Pacijent je tokom pregleda otkrio trombocitopatiju. Navedite koje promjene igraju važnu ulogu u patogenezi trombocitopatije?
@ Proizvodnja koštane srži patoloških trombocita
Smanjena antikoagulantna aktivnost
Hiperaktivacija trombocitopoeze
Povećana koncentracija prokoagulanata u krvi
Inhibicija fibrinolize.
Prije operacije, utvrđeno je da je kod ljudi vrijeme krvarenja povećano na 10 minuta. Koji nedostatak formiranih elemenata u krvi može izazvati takve promjene?
@ Broj trombocita
Crvene krvne ćelije
Monociti
Limfociti
Broj belih krvnih zrnaca
Kod pacijenta, produžena upotreba aspirina uzrokovala je krvarenje. Cilj: trombocitopenija sa smanjenom funkcionalnom aktivnošću trombocita. Trombocitopatija u ovom slučaju je uzrokovana inhibicijom aktivnosti:
@ Ciklo-oksigenaza
Citokrom oksidaza
Lipooxygenase
Superoksid dismutaza
Fosfolipaza A 2.
Pacijentu je dijagnosticirano smanjenje produkcije vaskularnog faktora vaskularnog endotela von Willebrand. Koja je povreda krvožilne vaskularne hemostaze uočena u ovom slučaju?
@ Kršenje adhezije trombocita
Poremećaj agregacije trombocita
Hiperkoagulacija
Povreda polimerizacije fibrina
Jačanje fibrinolize
Dijete sa hemoragijskim osipom koje se desilo nakon akutne respiratorne virusne infekcije je dijagnosticirano hemoragijskim vaskulitisom (Henlinova bolest). Alergijske reakcije koje vrste (prema Coombsu i Jelli) su osnova ove bolesti?
Tip III (imunokompleks)
Tip I (anafilaktički)
Tip II (humoralna citotoksična)
Tip IV (stanični citotoksični)
Tip V (stimulirajući)
Dijete sa hemoragijskim osipom koje se desilo nakon akutne respiratorne virusne infekcije je dijagnosticirano hemoragijskim vaskulitisom (Henlinova bolest). Šta uzrokuje poremećenu hemostazu u ovoj bolesti?
@ Oštećenje vaskularnog zida
Nasledni defekt vezivnog tkiva vaskularnog zida
Nasljedni nedostatak antikoagulanta
Inhibicija fibrinolize
Nasledni nedostatak prokoagulanta
Žena koja boluje od žučnog kamenca ima hemoragijski sindrom zbog nedostatka vitamina K. Koji od sledećih faktora nije adekvatan za hipovitaminozu K?
@ Stuart - Prouer (f. X)
Von Willebrandov faktor
Stabilizacija fibrina (f. XIII)
Fibrinogen (f. I)
Trombofilija (ubrzanje koagulacije krvi) otkrivena je kod pacijenta tokom pregleda. Šta može prouzrokovati kršenje?
@ Nedostatak inhibitora proteolitičkih enzima
Povećanje koncentracije prostaciklina
Smanjena koncentracija trombina u krvi
Povećanje koncentracije heparina u krvi
Povećanje koncentracije fibrinolizina u krvi
Pacijent sa oboljenjem jetre ima smanjenje količine protrombina u krvi. Ovo će dovesti do kršenja iznad svega:
@ Druga faza koagulacijske hemostaze
Fibrinolysis
Treća faza koagulacijske hemostaze
Vaskularna trombocitna hemostaza
Prva faza koagulacijske hemostaze
Dječak od 7 godina, nakon pada s bicikla, pojavila se hemartroza koljena. Uvođenje krioprecipitata i pumpanje krvi iz zgloba dovelo je do značajnog poboljšanja stanja djeteta. Na koju bolest mislim?
@Hemophilia A
Hemorrhagic vasculitis.
Trombocitopatija
Trombocitopenija
Reumatoidni artritis
Dečak sa izraženim hemoragijskim sindromom u krvnoj plazmi odsutan je antihemofilija globulin A (faktor VIII). Koja je primarna faza hemostaze kod ovog djeteta?
@ Unutrašnji put aktivacije protrombinaze
Povlačenje krvnog ugruška
Aktivacija eksternog puta protrombinaze
Dečak pati od hemofilije. Koji klinički znaci poremećaja koagulacijske hemostaze?
Petehijalno krvarenje
Microhematuria
Ekhimoza (modrice)
Oštećenje vida
@ Hematomas, produženo krvarenje
Žrtva nezgode neko vrijeme nakon što je pretrpjela poli traumom razvijen sindrom diseminirane intravaskularne koagulacije (DIC). Koji je faktor bio inicijator ove komplikacije?
@ Tromboplastin tkiva (f. III)
Fibrinogen (f. I)
Antihemofilni globulin A (f. VIII)
Pacijent sa akutnim pankreatitisom razvio je sindrom diseminirane intravaskularne koagulacije (DIC). Koja je supstanca bila inicijator ove komplikacije?
@ Trypsin
Fibrinogen (f. I)
Antihemofilni globulin A (f. VIII)
Stuart Factor - Prauera (f. X)
Antihemofilni globulin B (f. IX)
Kod bolesnika sa poli traumom i akutnim zatajenjem bubrega, stanje je komplikovano unutrašnjim krvarenjem. Koja je glavna karika u patogenezi ove faze DIC-a?
@ Potrošnja faktora zgrušavanja krvi
Oslobađanje leukocita iz depoa
Trombocitoza
Aktivacija protrombinaze
Inhibicija fibrinolize
Pacijent sa opekotinom razvio je DIC sindrom kao komplikaciju. Na koju fazu DIC sindroma se može sumnjati ako se zna da se krv pacijenta koagulira za manje od 3 minute?
@Hypercoagulation
Hypocoagulation
Oporavak
Latentno
Terminal
Pacijent sa povredom razvio DIC - sindrom. Koje promjene u hemostazi su uočene u drugoj fazi DIC sindroma?
@Hypocoagulation
Hiperkoagulacija.
Fibrinolysis
Trombocitopenija
Trombocitopatija
Pacijent nakon transfuzije nespojive krvi imao je DIC - sindrom. Koja je glavna karika u patogenezi ove komplikacije kod hemolize?
@ Unos intracelularnih proteaza krvi
Akumulacija bilirubina u krvi
Tromboplastin viška krvi
Višak protrombina u krvi
Povećanje sadržaja plazminogena
Pacijent sa hroničnom bubrežnom insuficijencijom razvio je DIC. Pregledom je utvrđeno povećanje vremena zgrušavanja krvi, trombocitopenija, povećanje nivoa kompleksa fibrin-monomer i produkata degradacije fibrina. Na kojoj fazi ICD sindroma treba da mislim?
@Hypocoagulation
Hypercoagulable
Oporavak
Latentno
Nestabilan
Pacijent sa hroničnom limfocitnom leukemijom razvio je hemoragije kao rezultat razvoja DIC sindroma. Koje će se promjene u perifernoj krvi promatrati?
@Hipokagulacija, trombocitopenija
Eritrocitoza, povećana viskoznost krvi
Trombocitoza, smanjenje vremena zgrušavanja krvi
Hiperkoagulacija, povećana agregacija trombocita
Prokoagulanti povećavaju aktivnost
Žena sa sepsom razvila je petehijalna krvarenja, smanjen broj trombocita i nivo fibrinogena u krvi, a pojavili su se i proizvodi razgradnje fibrina. Šta bi mogao biti uzrok značajnih promena?
@DIC sindrom
Leukopenija
Limfopenija
Trombocitoza
