Zvýšená hemostáza. Úplné vyliečenie sa nestane. Všetky podmienky terminálu, zastavenie srdca

Pacient s kurva má krvácanie z ďasien a petechie na koži. Čo spôsobuje zhoršenú hemostázu v tejto chorobe?
A. @ Porušenie syntézy kolagénu
B. Trombocytopénia
C. Prebytok antikoagulancií
D. Aktivácia fibrinolýzy
E. Nedostatok prokoagulantu
Chlapec s hemoragickým syndrómom nemá v krvi antihemofilný globulín A (faktor VIII). Aký mechanizmus hemokoagulácie má tento pacient?
@ Vnútorný mechanizmus tvorby protrombinázy
Premena fibrinogénu na fibrín
Externý mechanizmus tvorby protrombinázy
Konverzia protrombínu na trombín
Zrážanie krvných zrazenín
Muž, ktorý už dva roky trpel chronickou myeloidnou leukémiou, bol hospitalizovaný v stave akútneho zlyhania obličiek. Čo by mohlo byť príčinou akútneho zlyhania obličiek u tohto pacienta?
@ DIC - syndróm
lymfopénia
neutropénia
trombocytopénia
Nedostatočná aktivita akýchkoľvek koagulačných faktorov spôsobuje vývoj hemoragického syndrómu u pacientov s hypovitaminózou K?
X, IX, VII, II
Faktor von Willebrandovej
Pacient, ktorý systematicky konzumoval kyselinu acetylsalicylovú, vyvolal krvácanie. S poklesom aktivity, v ktorej sú v tomto prípade asociované trombocytopatia s trombocytárnymi enzýmami?
@ Cyklo-oxygenázy
lipoxygenázy
peroxidáza
Cytochrózooxidáza
Glukóza - 6 - fosfátdehydrogenáza
Dievča pravidelne krváca z nosa, na koži je malá hemoragická vyrážka. Skúmanie odhalilo: čas krvácania - 10 minút, znížená schopnosť adhéznych doštičiek a nízka aktivita f. VIII (VIII: C). Aká je choroba u dieťaťa?
@ Von Willebrandova choroba
Hemofília A
Hemofília B
Dedičná dysfibrinogénia
trombocytopénia
Po utrpení bolesti v krku má päťročná dievčina petechickú vyrážku na koži svojho trupu a končatín a krváca z ďasien. Skúmaním sa zistilo zníženie počtu krvných doštičiek. Na akej úrovni trombocytopénie (g / l) sa objavujú jej klinické príznaky?
Čo môže byť hlavným článkom v patogenéze trombofílie u pacienta trpiaceho tromboflebitídou dolných končatín?
@ Nedostatok antikoagulancií
trombocytopénia
thrombocytopathy
Prokoagulačný deficit
Aby bolo možné diagnostikovať, aký posun v systéme hemokoagulácie je predpísaný štúdiou hladiny produktov degradácie fibrínu v krvi?
thrombocytopathy
trombocytopénia
Vasopatia hemoragická
Pacient bol diagnostikovaný s genetickým defektom v membránovom receptore faktora von Willebranda - glykoproteínu (GP) Ib, ktorý je zodpovedný za počiatočný stupeň adhézie krvných doštičiek ku kolagénu. Aký je názov tejto choroby?
@ Bernard - Soulier
Von Willebrand
Addison - Birmera
Wilson - Konovalová
Glantsmana - Negeli
Pacienta bol diagnostikovaný dedičný defekt GP IIb - IIIa - membránový receptor, ktorý zabezpečuje spojenie fibrínu s membránou doštičiek a je potrebný na ich agregáciu. O akej chorobe hovoríme?
@Glancman - Negeli
Von Willebrand
Addison - Birmera
Wilson - Konovalová
Bernard - Soulier
U detí s kombinovanou imunodeficienciou krvný test ukázal pokles adhézie krvných doštičiek na kolagén, ich agregáciu, oslabenie koagulácie krvi a zrážanie krvných zrazenín. Pod ktorou imunodeficienciou sú pozorované podobné zmeny?
@ Whiskott - Aldrich
Švajčiarsky typ
Di - Georgie
Nezelofa
Chorému dievčaťu bola diagnostikovaná Glantsmannova trombasténia. Aké je poškodenie hemostatického systému?
@Disagregačná trombocytopatia
Absolútna trombocytopénia
Neprípustná trombocytopatia
Nedostatočná trombocytopatia
Trombocytopatia s distegranuláciou
Členovia expedície, ktorí sa nachádzali na severe, sa sťažujú na krvácanie z gingiva a petechiálne krvácanie na koži. Z anamnézy je známe, že strava nemá dostatok kyseliny askorbovej a to viedlo k krehkosti cievnej steny. Aká je patogenéza vasopatie?
@ Dysplastic
poburujúce
metaplastická
dystrofné
imúnny
U pacienta po dlhej operácii na pankrease sa pooperačná rana dlho krváca. Podľa koagulogramu sa zistilo významné zvýšenie hladiny plazmínu. Aká je patogenéza koagulopatie v tomto prípade?
@ Fibrinopathy
Protrombinazopatiya
Tromboplastinopatiya
Trombinopatiya
Vazopatiya
Pacientovi bola diagnostikovaná genetická chyba faktora V, ktorá je necitlivá na inaktiváciu antitrombotickým komplexom trombomodulínu - proteínu C, ktorý znižuje schopnosť cievnej steny obmedziť tvorbu fibrínu. Akú patológiu koagulácie krvi vznikne s touto anomáliou?
@ Thrombophilia
trombocytopénia
thrombocytopathy
Hemoragický syndróm
Kľúčové pojmy narušenej hemostázy:
1. Poruchy hemostázy, koagulopatia (koagulopatia, koagulo- + grécky patos - utrpenie, choroba) - porucha funkcie koagulačných a antikoagulačných systémov krvi.
2. Hyperkoagulačný trombotický stav- stav sprevádzaný patologickým procesom zvýšenej zrážanlivosti krvi v dôsledku zvýšenej agregácie krvných doštičiek, aktiváciou plazmatických a tkanivových koagulačných faktorov s tvorbou krvných doštičiek a fibrínových zrazenín.
3. Hypokoagulačný hemoragický stav- Stav, ktorý je sprevádzaný patologickým procesom znižovania zrážanlivosti krvi v dôsledku zníženia agregácie doštičiek, inaktivácie faktorov zrážania plazmy a tkaniva s výskytom krvácania a krvácania.
4. DIC syndróm (trombotický hemoragický stav) - syndróm diseminovanej intravaskulárnej koagulácie krvi - typický patologický proces poškodenia hemostázy v dôsledku toho, dystrofiu vnútorných orgánov.
V akých chorobách dochádza k porušeniu hemostázy:Hemostáza je komplexný proces, ktorý zabraňuje alebo zastavuje odtok krvi z lumen cievy, zaisťuje konvoluciu fibrínu potrebnú na obnovenie integrity tkaniva a nakoniec odstraňuje fibrín, keď zmizne jeho potreba. V tomto procese sú zapojené štyri hlavné fyziologické mechanizmy.
Použitie krv hemostatický systém plní svoju dôležitú funkciu - udržanie kvapalného skupenstva krvi prúdiacej v cievach, a koagulácie krvi tým, poškodenie cievnej steny, a tým zastavenie krvácania a udržanie objemu krvi a zloženie. Systém hemostázy je viaczložkový. Jedná sa krvné doštičky a ostatné krvné bunky, cievne steny extravaskulárnej tkaniva, biologicky aktívnych látok (na doštičky vaskulárne hemostázy), v plazme, tkanivové faktory zrážanlivosti (koagulácia hemostázy) úzko leží s antikoagulantom, fibrinolytickej a kalikreín-kinínového systémy. Porušenie ktorejkoľvek z týchto zložiek vedie k patológii hemostázy.
Klasifikácia porúch hemostázy. Patológia hemostázy je klasifikovaná podľa prevládajúcej lézie jej rôznych zložiek na porušenie vaskulárnej hemostázy krvných doštičiek a koagulačnej hemostázy. Podľa etiológie týchto porúch môžu byť získané a dedičné, a na smere zmien rozdelených do zníženie zrážania krvi (hypocoagulation) a zvýšenie krvnej zrážanlivosti (hyperkoagulability), ktorý môže byť lokálna (trombóza) a generalizované (DIC).
Zníženie koagulácie krvi
Pokles koagulácie krvi sa prejavuje zvýšeným krvácaním (hemoragický syndróm) - opakované krvácanie, krvácanie, ktoré vznikajú spontánne aj s malými poraneniami.
Krvotvorná cievna hemostáza je narušená kvantitatívnymi a kvalitatívnymi zmenami krvných doštičiek (trombocytopénia a trombocytopatia), ako aj lézie cievnej steny.
Trombocytopénia sa nazýva pokles počtu krvných doštičiek v krvi pod normou (180-320 G / l alebo 180-320x109 / l). Spontánne krvácanie sa však vyskytuje len vtedy, keď ich počet klesne pod 30 G / l. Pod trombocytopatiami rozumie kvalita podradnosti a dysfunkcie krvných doštičiek s normálnym alebo zníženým obsahom.Príčiny nízkej krvnej zrážanlivosti. Príčinou trombocytopénia imunitných odpovedí sú často mení antigénne štruktúru krvných doštičiek pôsobením vírusov, lieky, antiagregačné autoprotilátky formulácie (s chronickou lymfatickou leukémiou, idiopatickej trombocytopénie), krvných doštičiek nezlučiteľnosti medzi matkou a antigény plodu. Okrem toho sa trombocytopénia vyvíja kvôli porušeniu megakaryocytového vývinu kostnej drene ionizujúcim žiarením, chemikáliami alebo ich nahradením nádorovými metastázami, leukemickými infiltrátmi. Zníženie trombocytopoézy môže byť spôsobené nedostatkom kyanokobalamínu a kyseliny listovej, dedičnou poruchou tvorby krvných doštičiek (vrátane tých, ktoré majú nedostatok trombocytopoetínov). Z toho vyplýva trombocytopénia mechanické poškodenie krvných doštičiek so splenomegáliou, umelých srdcových chlopní, ako aj zvýšenej spotreby krvných doštičiek s lokálnou a generalizovanou intravaskulárnou koaguláciou krvi.
Etiologické faktory spôsobujúce trombocytopatiu zahŕňajú pôsobenie toxických látok a liečiv (alkohol, kyselina acetylsalicylová), ionizujúce žiarenie, endogénne metabolity (uremia, cirhóza pečene); deficiencia cyanokobalamínu, hormonálne poruchy (hypotyreóza). Existujú aj genetické defekty štruktúry membrány a biochemické zloženie krvných doštičiek (nedostatok trombostenínu, faktor 3, ATP, ADP, G-6-FDG, membránové receptory pre faktory V, VIII, XI atď.).Hemoragické vazopatiyah lézie cievnej steny, čo vedie k narušeniu doštičky vaskulárnej hemostázy a krvácanie, dochádza v dôsledku zvýšenej permeability steny krvných ciev a jeho degradácii v rozpore s syntézu kolagénu (pre potravinárske nedostatku kyseliny askorbovej, vrodených chýb v syntéze kolagénu) pôsobením biologicky aktívnych látok ( alergia), rádiotoxíny (ožarová choroba), imunitná hemoragická vaskulitída, zníženie angiotrofnej funkcie krvných doštičiek počas trombocytov Otvorenie a thrombocytopathy, zničenie leukemické infiltráciu cievnej steny. Jednou z príčin krvácania je pokles produkcie vaskulárnej steny endotelu von Willebrandovho faktora - zložky s veľkou molekulou koagulačného faktora VIII - krvi (dedičná choroba von Willebrandovej choroby). Tento faktor sa hromadí v krvných doštičkách a pri degranulácii sa uvoľňuje.
Pre normálnu priľnavosť krvných doštičiek ku kolagénovej stene je nevyhnutné a bez nej sa nevytvorí trombóm krvných doštičiek. Hemoragický syndróm sa pozoruje aj vtedy, keď sa zvýši membránová peroxidácia membránových fosfolipidov, v dôsledku čoho sa v endotelu syntetizuje a vylučuje nadmerné množstvo silných inhibítorov agregácie trombocytov, prostacyklínov. Okrem toho zhoršená neurogénna a humorálna regulácia vaskulárneho tónu vedie k zníženiu vaskulárnej hemostázy krvných doštičiek, čo vedie k nemožnosti blokovania malých ciev trombocytárnym trombom.
Patogenéza nízkej koagulácie krvi. Existujú štyri hlavné mechanizmy trombocytopénie: pokles produkcie, zvýšená deštrukcia, zvýšená spotreba (trombóza), prerozdelenie krvných doštičiek.
Prerušenie hemostázy a vývoj krvácania počas trombocytopénie v dôsledku nasledujúcich mechanizmov:
- zvýšená mikrovaskulárna priepustnosť erytrocytov a iných krvných zložiek (diapedemické krvácanie) a vaskulárna krehkosť v dôsledku dystrofie steny pri vypnutí funkcie angiotrofných krvných doštičiek;
- zníženie funkcie adhéznej agregácie doštičiek;
- porušenie reakcie uvoľňovania krvných koagulačných faktorov krvných doštičiek, ADP, serotonínu, adrenalínu, antiheparínového faktora, čo vedie k nedostatočnej tvorbe krvných doštičiek, absencii vazospazmu a spomaleniu koagulácie;
- zníženie zrážania zrazeniny v dôsledku zníženia aktivity kontraktilného trombocytového proteínu, trombostenínu (trombocytový faktor 8).V patogenéze trombocytopatie je možné rozlíšiť dva hlavné mechanizmy ich výskytu: produkcia patologických krvných doštičiek v kostnej dreni a deštrukcia krvných doštičiek vo všetkých častiach krvného systému. Patogenéza trombocytárnej hemostázy s trombocytopatiou je rovnaká ako pri trombocytopénii, pretože je spojená s deaktiváciou funkcií krvných doštičiek.
Porušenie koagulačnej hemostázy vedúce k vzniku krvácania môže byť spôsobené nasledujúcimi faktormi:
- získané a dedičné zníženie alebo skreslenie syntézy koagulačných faktorov plazmy a krvných doštičiek a zložiek systému kalikreín-kinín;
- inhibíciu alebo zvýšenú spotrebu týchto faktorov;
- zvýšenie endogénnych antikoagulancií;
- aktivácia fibrinolytického systému;
- Predávkovanie antikoagulanciami, fibrinolytickými a defibrinujúcimi liekmi. Toto všetko je základom porušenia jednej z troch fáz krvnej koagulácie a zrážania krvných zrazenín alebo ich kombinovanej zmeny.Príčiny porušenie prvej fáze zrážania krvi - tvorba tromboplastínu - ich budú produkty redukcia faktorov (IX, X) v patológiu pečene, tvorba protilátok proti niektoré faktory (VIII, IX) v ochorení, patogenézy, ktorý má autoimunitné zložku (leukémia, kolagén) alebo predávkovanie takého univerzálneho antikoagulantu ako heparínu. V syntéze faktorov VIII, IX a XI sú známe genetické defekty, ktorých nedostatok je základom pre vývoj hemofílie (sekvencia týchto faktorov je hemofília A, B a C).
Porušenie druhej fázy zrážania krvi - trombínu - dochádza nielen pre choroby pečene, ale aj v hypo- a beriberi K pri znížený príliš syntézu v pečeni faktorov II, V, VII, zapojený v tejto fáze (s obštrukciou, enteritída, rozsiahle resekcia tenkého čreva, liečivá dysbakterióza). Výskyt inhibítorov imunitného faktorov V, VII (napríklad pri liečbe streptomycín sulfátu), zvýšili ich vylučovanie obličkami, dedičným deficitom (faktor V, keď paragemofilii) alebo inaktiváciu komponenty antikoagulačný systém - antitrombínu, heparín (s anafylaktický šok, predávkovanie heparínu).
Hemoragická diatéza spojená s poruchou koagulácie tretia fáza - fáza tvorby fibrínu dochádza znížením syntézy fibrinogénu v infikovaných pečene patologického procesu, svetla alebo v dôsledku dedičné hypo-, afibrinogenemia a fibrinstabiliziruyuschego nedostatočnosť faktora (faktor XIII). Avšak výrazne častejšie je porušenie tretej fázy dôsledkom zvýšenej fibrinolýzy pri traume (operácii) pľúc, maternice, pankreasu; popáleniny, šok. To je v dôsledku zvýšenej krv vstupuje do aktivátora plazminogénu (plazminogénu) - tkaniva, mikrobiálne fibrinokinaz, leuko- a erytrocytov aktivátory, zložiek kalikreín-kinínového a systém komplementu heparínových komplexy s fibrinogén, plazminogén a adrenalínu (tieto komplexy poskytujú neenzymatické fibrinolýzu B. A . Kudryashov).
Patogenéza. Hlavné väzby v patogenéze hemoragickej diatézy, ktoré sa vyvinuli v rozpore s niektorou z fáz krvnej zrážanlivosti, sú chronická krvná strata a jej následky, ako aj štrukturálne a funkčné zmeny v mieste krvácania (v kĺboch, vnútorné orgány, kože a iných tkanív).
Zvýšená koagulácia krvi
Zvýšenie koagulácie krvi sa prejavuje lokálnou (trombózou) alebo generalizovanou intravaskulárnou koaguláciou krvi, založenou na porušení trombocytárnej a koagulačnej hemostázy.Hyperkoagulácia môže byť spôsobená:
- zvýšenie funkčnej aktivity krvného koagulačného systému v dôsledku zvýšeného príjmu prokoagulancií a aktivátorov zrážania krvi do krvi;
- zvýšenie obsahu krvných doštičiek;
- zníženie antitrombotických vlastností cievnej steny;
- zníženie aktivity krvného antikoagulačného systému;
- oslabenie fibrinolýzy.Všeobecnej (rozšírené) intravaskulárna koagulácia (DIC), - závažná porucha hemostázy, ktorý sa vyskytuje pri prekročení bezprostrednej krvný procoagulants a aktivátory koagulácia, ktoré vedú k tvorbe viac mikrotrombov v cievach mikrocirkuláciu a potom vývoj hypocoagulation, trombocytopénia a krvácanie vedie "spotreba" faktorov koagulačného systému a zvýšenie funkčnej aktivity antikoagulačného systému a fibrinolýzy krvi s následným vyčerpaním všetkých t EX systémy.
Etiológie. Univerzálnosť a nešpecifikácia DIC je spôsobená rôznorodosťou kauzálnych faktorov jeho výskytu. Patrí medzi ne predovšetkým zovšeobecnené infekcií a septických stavov, všetky druhy šoku, úrazovej chirurgie, pôrodníckej patológie (predčasné odlúčenie, ručné odstránenie placenty), akútna intravaskulárnej hemolýzy, urémia v zlyhanie obličiek, všetky koncové stavy.
Patogenéza. Hlavný odkaz v patogenéze generalizované hyperkoagulovatelné je nerovnováha medzi kalikreín-kinínového, koagulácie, antikoagulačnej a fibrinolytického systému v krvi pri vstupe do krvného obehu veľké množstvo prokoagulačnej a aktivátorov. To vedie k narušeniu krvi tak dôležitú funkciu ako zachovanie normálneho stavu agregácie, čo vedie k fáze hyper koaguláciu krvných zrazenín v cievach a zastaví jej pohyb s rozvojom ťažkých degeneratívnych a funkčných porúch v orgánoch a tkanivách sú často nekompatibilné so životom. V následnej fáze hypokoagulácie spôsobuje zriedenie krvi a strata schopnosti zrážať a agregovať krvné doštičky krvácanie, ktoré je zle podliehajúce terapeutickej korekcii. S priaznivým výsledkom prichádza tretí - fáza obnovy, pri ktorej sa normalizuje hemostáza.
Stav hemostázy určuje priebeh a výsledok tehotenstva pre matku a plod. V posledných rokoch došlo k značné množstvo publikácií, čo naznačuje dôležitú úlohu trombofilná komplikácií obvyklé potrat, úmrtie plodu, odtrhnutie placenty, pri rozvoji preeklampsia, vnútromaternicové rastové retardácie.
Hlavné mechanizmy hemostázy
Systém hemostázy alebo systém regulácie agregačného stavu krvi (PACK) je biologický systém, ktorý reguluje stav agregácie krvi a udržuje hemostatický potenciál potrebný pre organizmus. Systém PACK je mozaika, t.j. hemostatický potenciál v rôznych častiach prietoku krvi nie je rovnaký. Táto podmienka je normálna pre funkčný systém, Systém regulácie agregačného stavu krvi zahŕňa:
- centrálne orgány systému - kostná dreň, pečeň, slezina;
- periférne formácie - žírne bunky, endometrium a ďalšie vrstvy cievnej steny, krvné bunky;
- miestne regulačné systémy - vegetatívny nervový systém, subkortikálne štruktúry.
Systém hemostázy je regulovaný komplexnými neurohumorálnymi mechanizmami. Tieto mechanizmy vytvárajú podmienky, pri ktorých miestny proces zrážania kože, ktorý je nevyhnutný na zastavenie krvácania, neprejde do procesu všeobecnej intravaskulárnej koagulácie počas normálneho fungovania systému.
V systéme hemostázy sú štyri hlavné odkazy:
- Cievne trombocytárne spojenie;
- hemostatický;
- Fibrinolytické spojenie;
- Link inhibítory koagulácie.
Vaskulárne krvné doštičky
Systém hemostázy trombocytov je často označovaný ako primárna hemostáza. Endotelium krvných ciev hrá dôležitú úlohu pri udržiavaní agregačného stavu cirkulujúcej krvi. Je to spôsobené nasledujúcimi funkciami:
- schopnosť tvoriť a uvoľňovať do krvi silný inhibítor agregácie krvných doštičiek - prostacyklín (metabolit kyseliny arachidónovej);
- produkcia tkanivového fibrinolýzového aktivátora;
- neschopnosť kontaktovať aktiváciu systému zrážania krvi;
- vytvorenie antikoagulačného potenciálu v rozhraní krvi / tkaniva fixáciou komplexu heparínu-antitrombínu III na endotel;
- schopnosť odstrániť aktivované faktory zrážania z krvného riečišťa.
Zapojenie doštičiek v hemostázy je určená ich schopnosťou adherovat na mieste poškodením endotelu, proces ich agregácie a tvorba zátky primárnych krvných doštičiek, ako aj ich schopnosť udržiavať vaskulárny spazmus sekréciou vazoaktívnych látok -. Adrenalín, norepinefrín, serotonín, ADP, atď., A tiež tvoriť, zhromažďujú a vylučujú látky, ktoré podporujú priľnavosť a agregáciu.
Preto početné štúdie viedli k záveru, že primárna hemostáza sa uskutočňuje hlavne krvnými doštičkami a nie krvnou koaguláciou. Vedúca úloha pri realizácii primárnej hemostázy patrí do funkcie adhéznej agregácie krvných doštičiek.
Adhézia - adhézia krvných doštičiek na miesto poškodenia cievnej steny, kolagénové vlákna cievnej steny, mikrofibrín a elastín. Najdôležitejšími plazmatickými kofaktormi tohto spôsobu sú ióny vápnika a syntetizovaný vaginálnym faktorom v endotelovom proteíne a doštičkových membránových glykoproteínoch. Fyziologický účel adhézie - uzatvorenie defektu v cievnej stene. Súbežne s adhéziou dochádza k agregácii trombocytov. Zároveň sa krvné doštičky nielen zlepú spoločne, ale tiež prilepia na prilepené krvné doštičky, čím sa vytvorí hemostatická zátka. V procese adhézie a agregácie sa krvné doštičky z krvných doštičiek aktívne sekvestrujú granuly obsahujúce látky, ktoré zlepšujú proces agregácie a tvoria jej druhú vlnu. Reakcia uvoľnenie doštičiek faktorov -. ADP, epinefrín, norepinefrín, serotonín, antigeparinovogo faktor, beta-thromboglobulin, atď. Neskôr vylučovaný granule obsahujúce lysozomálnych enzýmy (uvoľňovacej reakcie II). Výťažok je adrenalín, noradrenalín a sérotonín nielen zvyšuje agregáciu, ale tiež prispieva k sekundárnej kŕčov ciev, ktoré je sprevádzané fixačná spoľahlivé zátkou doštičiek v mieste cievneho poranenia. Interakcia krvných doštičiek a plazmových faktorov hemostázy zóny vytvorené trombín, ktorý nielen zvyšuje agregáciu doštičiek, ale aj stimulátor zrážanie krvi tvorený fibrínové zrazeniny formy, ktorá sa stáva hustá a nepriepustné pre plazme a srvátky, je jeho zatiahnutie.
Do veľkej miery sa mechanizmus agregácie doštičiek objavil po objavení prostaglandínov v krvných doštičkách a cievnej stene. Rôzne agregačné činidlá aktivujú fosfolipázu A1, ktorá spôsobuje odstránenie kyseliny arachidónovej z fosfolipidov, čo je silná agregujúca látka. Pod vplyvom prostaglandín syntetázy sa vytvárajú cyklické endosperoxidy prostaglandínov, ktoré stimulujú kontrakciu fibríl v krvných doštičkách a majú silný agregačný účinok. Pod vplyvom tromboxán syntetázy sa tromboxán A1 syntetizuje do krvných doštičiek. Táto látka prispieva k transportu Ca2 + v krvných doštičkách, čo vedie k tvorbe ADP - hlavného stimulátora endogénnej agregácie. Úroveň cAMP-univerzálneho biologického nosiča je regulovaná adenylátcyklázou, ktorá katalyzuje reakciu ATP-cAMP.
Podobný proces sa vyskytuje v cievnom endotelu - prostaglandíny endoperoxidy sú tvorené z kyseliny arachidónovej pod vplyvom prostaglandín syntetázy. Ďalej sa pod vplyvom prostacyklínsyntetázy tvorí prostacyklín (prostaglandín L), ktorý má silný dezagregačný účinok a aktivuje adenylátcyklázu.
Tak, tzv. tromboxán - prostacyklínová rovnováha - jeden z hlavných regulátorov stavu cievneho stenového tkaniva a agregácie trombocytov.
Procoagulant Link hemostáza
V procese zrážania krvi sa zúčastňujú zlúčeniny obsiahnuté v plazme (prokoagulanty). Ide o komplexný viacstupňový enzymatický proces, ktorý sa dá rozdeliť do troch etáp.
- Stupeň I - komplex reakcií, ktoré vedú k tvorbe protrombínového aktívneho komplexu alebo protrombinázy. Komplex zahŕňa faktor X, tretí faktor trombocytov (fosfolipid), faktor V a Ca2 + ióny. Toto je najťažšia a najdlhšia fáza.
- Stupeň II - pod vplyvom protrombinázy protrombín ide do trombínu.
- Stupeň III - pod vplyvom trombínu prechádza fibrinogén do fibrínu.
Kľúčovým bodom pri tvorbe protrombinázy je aktivácia koagulačného faktora X, ktorý sa dá dosiahnuť dvomi hlavnými mechanizmami spúšťania koagulačného procesu - vonkajšieho a vnútorného.
S externým mechanizmom je koagulácia stimulovaná vstupom tkanivového tromboplazmínu (III alebo komplexu fosfolipid-apoproteín III) do plazmy. Tento mechanizmus sa určuje protrombínovým testom času (PT).
S vnútorným mechanizmom zrážania sa vykonáva bez účasti tkanivového tromboplastínu. Spúšťacím faktorom pre túto koagulačnú dráhu je aktivácia faktora X. Aktivácia faktora X sa môže vyskytnúť v dôsledku kontaktu s kolagénom v prípade poškodenia cievnej steny alebo dráhy enzýmu pod vplyvom kalikreínu, plazmínu alebo iných proteáz.
Tak s vonkajšou, ako aj s vnútornou koagulačnou cestou sa interakcia a aktivácia faktorov uskutočňuje na fosfolipidových membránach, na ktorých sú fixované koagulačné faktory proteínov pomocou iónov Ca.
Nomenklatúra plazmatických koagulačných faktorov:
- I - fibrinogén;
- II - protrombín;
- III - tkanivový tromboplastín;
- IV - vápnik;
- V - akceleračný faktor;
- VI - aktivátor faktora V;
- VII - prokonvertin;
- VIII - antihemofilný globulín A;
- IX - antihemofilný faktor B (vianočný faktor);
- X-protrombináza;
- XI - prekurzor plazmatického tromboplastínu;
- XII - faktor Hageman;
- XIII - fibrinázu.
Vonkajšie a vnútorné mechanizmy aktivácie krvného koagulačného systému nie sú navzájom izolované. Zahrnutie medzi nimi "mostíkov" slúži ako diagnostický znak pri rozpoznávaní intravaskulárnej aktivácie koagulačného systému. Pri analýze výsledkov hlavných koagulačných testov je potrebné zvážiť:
- Medzi koagulačnými faktormi plazmy participuje iba faktor VII na vonkajšom koagulačnom mechanizme a ak je nedostatočný, predlžuje sa iba protrombínový čas.
- Faktory XII, IX, XI, VIII a prekalikreín sa podieľajú iba na vnútornom mechanizme aktivácie, v súvislosti s ktorým sú nedostatočné v APTT a autokoagulačnom teste, zatiaľ čo protrombínový čas zostáva normálny.
- Pri nedostatku faktorov X, V, II, I, na ktorých sú uzavreté obidva mechanizmy zrážania, sa vo všetkých uvedených testoch zistí patológia.
Okrem vonkajších a vnútorných mechanizmov hemokoagulácie existujú v organizme dodatočné aktivačné cesty rezervy, ktoré sú zahrnuté na požiadanie. Najdôležitejšou cestou je makrofágový - monocytový mechanizmus hemokoagulácie. Ak sú aktivované endotoxínmi alebo inými infekčnými antigénmi, začnú tieto bunky vylučovať väčšie množstvo tkanivového tromboplastínu.
Endogénne inhibítory koagulácie
Na udržanie krvi v tekutom stave a na obmedzenie procesu trombózy sú potrebné fyziologické antikoagulancie. V súčasnosti je známe, že prírodné antikoagulanciá sú veľkou skupinou zlúčenín pôsobiacich na rôznych fázach hemostázy. Okrem toho množstvo antikoagulancií súčasne ovplyvňuje fibrinogenézu, tvorbu systému kalikreín-kinín, systém komplementu.
Prírodné antikoagulanciá sa delí na primárny, stále prítomný v plazme a vytvorených krvných elementov a pôsobí nezávisle od vzniku alebo rozpustenie krvnej zrazeniny, a sekundárne, ktoré vznikajú v procese zrážania krvi a fibrinolýzy, v dôsledku proteolytického pôsobenia enzýmu na substrát. Antitrombín III (AT III) predstavuje až 75% prirodzeného antikoagulačného potenciálu. Antitrombín III je schopný blokovať protrombinázu tak externými, ako aj vnútornými mechanizmami, pretože inhibítorom faktorov XIIa, XIa, IXa, VIIIa, kalikreínu, All sa viaže plazmín. Aktivita antitrombínu III sa zvyšuje viac ako 100-krát pri tvorbe komplexov s heparínom. Heparín nie je spojený s antitrombínom III, nemá antikoagulačný účinok. S poklesom hladiny antitrombínu III nastáva závažný trombofilný stav, ktorý sa vyznačuje recidivujúcou trombózou, pľúcnym tromboembolizmom a srdcovými záchvatmi. Keď sa antitrombín III zníži pod 30%, pacienti zomrú na tromboembolizmus a heparín nemá na krv antikoagulačný účinok. Nedostatok antitrombínu III vytvára rezistenciu voči heparínu.
Prírodné antikoagulanciá zahŕňajú proteín C, proteín S, alfa2-makroglobulín.
Proteín C je proenzým, aktivovaný trombínom a faktorom Xa. Aktivácia je v kombinácii s fosfolipidom a vápnikom. Proces je zvýšená pod vplyvom thrombomodulin a proteínu S, ktorá oslabuje schopnosť trombínu aktivovať faktory VIII a V. Pri deficiencie proteínu C označený sklon k trombóze, ktorá je pozorovaná v akútnom DIC, syndrómu respiračnej tiesne a ďalšie.
V procese zrážania krvi a fibrinolýzy sa v dôsledku ďalšej enzymatickej degradácie koagulačných faktorov vytvárajú sekundárne prírodné antikoagulanciá.
Patologické antikoagulanciá sú v krvi neprítomné normálne podmienkyAle objavujú v rôznych imunitných porúch, medzi ne patrí protilátky proti koagulačné faktory, najčastejšie na faktoroch VIII a V (často vyskytujú po pôrode a masívne transfúzia krvi a imunitný komplexy - lupus antikoagulans, antitrombín, V).
Fibrinolytický systém
Fibrinolytický systém pozostáva z plazminogénu a jeho aktivátorov a inhibítorov.
Aktivátory plazminogénu sú skupinou faktorov, ktoré premieňajú plazminogén na plazmín. Patria medzi ne takéto látky kakurokinázu, bakteriálne enzýmy. Aktívny plazmín je rýchlo blokovaný antiplazmínmi a eliminuje sa z krvného obehu. Aktivácia fibrinolýzy, ako aj aktivácia krvnej koagulácie sa uskutočňuje tak na vonkajšej, ako aj na vnútornej dráhe.
Vnútorná dráha aktivácie fibrinolýzy je určená rovnakými faktormi ako koagulácia krvi, t.j. faktorov XIIa alebo XIII s kalikreínom a kininogénom. Externá aktivačná dráha sa uskutočňuje na úkor aktivátorov tkanivového typu syntetizovaných v endotelu. Aktivátory tkanivového typu sa nachádzajú v mnohých tkanivách a telesných tekutinách, krvných bunkách. Inhibovaná fibrinolýza alfa2-antiplasmin globulín alfa2 makroglobulínu, antitrypsín a kol. Plasminu systém je prispôsobený na lyži zrazenín fibrínu (trombov) a rozpustný fibrín monomér komplexu (SfmC). A len vtedy, keď dôjde k nadmernej aktivácii lýzy fibrínu, fibrinogénu a ďalších proteínov. Aktívny plazmin spôsobuje postupné delenie fibrinogénu / fibrínu tvorbou ich degradačných produktov (PDF), ktorých prítomnosť indikuje aktiváciu fibrinolýzy.
Spravidla vo väčšine klinických pozorovaní je aktivácia fibrinolýzy sekundárna a je spojená s diseminovanou intravaskulárnou koaguláciou krvi.
V procese koagulácie a fibrinolýzy sa vyskytujúce sekundárne, prírodné antikoagulanciá - FDP odpadov a ďalších koagulačných faktorov - biologicky aktívne, ktoré fungujú ako antikoagulanty a inhibítory agregácie trombocytov.
V súčasnosti existujú imunitné trombofilné komplikácie a dedičné nedostatky hemostázy.
Systém hemostázy počas tehotenstva
Dominantným hľadiskom je, že v tehotnej žene sú vytvorené určité podmienky na rozvoj diseminovaného intravaskulárneho koagulačného syndrómu. To má za následok zvýšenie spoločné koagulačný úpravy (celkové aktivity koagulačných faktorov), zlepšenie funkčnú aktivitu krvných doštičiek s určitým znížením ich počtu, zníženie fibrinolytickej aktivity s rastúcou PDF, zníženie aktivity antitrombínu III v určitej zníženie jeho obsahu. Tieto znaky majú kompenzačnú a adaptačnú povahu a sú nevyhnutné pre normálnu tvorbu placentárneho komplexu, ako aj pre obmedzenie straty krvi počas pôrodu. Pri aktivácii systému hemostázy zohrávajú veľkú úlohu zmeny v celkovej hemodynamike tela tehotnej ženy. Pre normálne fungovanie systému placenty za vysokého koagulačné potenciálu krvi vstupujú do hry kompenzačných-adaptívne mechanizmy: zvýšenie počtu koncových klkov malého kalibru a periférnych umiestnenie hyperplázia kapilár, znižuje placentárnu hrúbka bariéra tvorbu syncytia riedenie sintsitiokapillyarnyh membrán syncytiálnych uzlov.
Funkcie funkcie hemostázy sú spojené s určitými zmenami v systéme špirálových tepien maternice. Tento - invázia trofoblastu v stene špirálových artérií, substitúcia vnútorné pružná membrána a vnútorné médiá silný fibrín, narušenie integrity endotelu a odizolovanie kolagénu subendoteliálnych štruktúry. V tomto procese je dôležitý aj vývoj intervilového priestoru s jeho vlastnými morfologickými a hemodynamickými vlastnosťami.
Charakteristiky systému hemostázy počas fyziologického tehotenstva sú determinované tvorbou uteroplacentárneho obehu.
Hladina krvných doštičiek s nekomplikovaným tehotenstvom zostáva takmer nezmenená, aj keď existujú štúdie, pri ktorých dochádza k poklesu hladiny krvných doštičiek. Pri znížení hladín krvných doštičiek pod 150000 / ml je potrebný výskum na identifikáciu príčin trombocytopénie.
Počas tehotenstva sa pozoruje zvýšenie koagulačného potenciálu, telo sa pripravuje na možné krvácanie počas pôrodu. Zaznamenal sa nárast všetkých koagulačných faktorov s výnimkou faktora XI a XIII.
Zvýšenie hladiny fibrinogénu začína od 3. mesiaca gravidity a napriek zvýšeniu objemu cirkulujúcej plazmy sa hladina fibrinogénu na konci tehotenstva zvyšuje najmenej dvakrát v porovnaní s netehotným stavom.
Aktivita faktora VIII (faktor von Willebrandovej) sa tiež zvyšuje nielen u zdravých žien, ale aj u pacientov - vodičov hemofílie a pacientov s von Willebrandovou chorobou. Treba mať na pamäti, že pri miernom a strednom stupni tejto choroby môže byť úroveň tohto faktora takmer normálna. Na rozdiel od všeobecného zvýšenia koagulačných faktorov sa v priebehu tehotenstva zaznamenal mierny pokles faktora XI na konci tehotenstva a výraznejší pokles faktora XIII (faktor stabilizujúci fibrín). Fyziologická úloha týchto zmien ešte nie je jasná.
Koagulačný potenciál krvi sa zvyšuje, aj keď hladina antitrombínu III klesá, proteín C stúpa najmä v popôrodnom období a proteín S sa počas tehotenstva zníži a významne sa zníži po pôrode.
Počas tehotenstva došlo k zníženiu fibrinolýzy na konci tehotenstva a počas pôrodu. V počiatočnom období po pôrode sa aktivita fibrinolýzy vráti do normálu. Existujú konfliktné údaje týkajúce sa prítomnosti FDP v krvnom riečisku. Podľa štúdie došlo k miernemu zvýšeniu FDP v posledných mesiacoch tehotenstva. Podľa výskumu s nekomplikovaným priebehom tehotenstva sa nezistil nárast obsahu degradačných produktov až do začiatku pôrodu. Podľa J. Rand a kol. (1991), úroveň niektorých fragmentov produktov degradácie fibrínu sa zvyšuje od 16 týždňov tehotenstva a dosiahne plató v 36-40 týždňoch. Avšak výrazné zvýšenie počtu PDF počas tehotenstva je pravdepodobne odrazom fibrinolytického procesu spôsobeného aktiváciou intravaskulárnej koagulácie.
Zmeny v systéme hemostázy u gravidných žien s antifosfolipidovým syndrómom
Parametre hemostatického systému u gravidných žien s antifosfolipidovým syndrómom sa významne líšia od parametrov u žien s fyziologickým tehotenstvom. Od nástupu tehotenstva má väčšina pacientov zmeny hemostázy doštičiek. Agregácia doštičiek počas stimulácie ADP je o 55-33% vyššia ako počas fyziologického tehotenstva. Tendencia zvýšenia agregácie pretrváva na pozadí antiagregačnej terapie.
Agregácia krvných doštičiek pod pôsobením kolagénu je 1,8-krát vyššia ako pri fyziologickom priebehu tehotenstva. Agregácia doštičiek adrenalínom je o 39% vyššia ako u kontrolnej skupiny. Ak pod vplyvom terapie nie je možné tieto indikátory znížiť, takáto pretrvávajúca hyperaktivita krvných doštičiek je základom pre zvýšenie dávky antiagregačných činidiel alebo predpísaním ďalších protidoštičkových látok. Ukazovatele ristomycínu - agregácie v priemere v prvom trimestri zostávajú v normálnom rozmedzí. Štúdie ukázali, že skorej fáze tehotenstva u pacientov s APS majú zvýšenú odpoveď doštičiek na účinky biologických induktorov určených predovšetkým v testoch doštičiek funkčnej aktivity, ako je napríklad agregácie pod vplyvom ADP 1x10 a 1x10 3 M 5M kyseliny arachidónovej.
Pri hodnotení kvalitatívne charakteristiky typov agregatogramm v každom pozorovaní zaznamenané žiadne disagregaci (reverzibilná agregáciu), keď je vystavená aj slabý stimul ADP 1 x 10 7 M. To je indikované zmenou profilu kriviek v smere takzvané "atypické" hyperfunkčnú agregatogramm.
Indikátory plazma hemostáza v I trimestri tiež zmenená v porovnaní s kontrolou: došlo k výraznému zrýchleniu AVR, aby tromboelastogramma skrátiť index r + k, čo je významne vyššia štrukturálne vlastnosti fibrínové zrazeniny - ITP.
Tak, tehotné APS Aj trimestri už bolo uvedené mierny Hyperkoagulácia v odkaze plazmy hemostázy, vyvíjajúci sa pred Hyperkoagulácia spojené s adaptačným hemostázy pri fyziologickom tehotenstve. Tieto zmeny, ktoré určujú hyperaktivitu hemostázy vo všeobecnosti v prvom trimestri gravidity, sa nepovažujú za patologickú aktiváciu tvorby intravaskulárnych trombov, pretože mimoriadne zriedkavo v tomto gestačnom veku sme pozorovali výskyt markerov DIC - produktov fibrínu a degradácie fibrinogénu (FDP). Obsah PDF v prvom trimestri neprekročil 2x10 g / l. Toto bolo základom na to, aby sa považovala hyperaktivita hemostázy krvných doštičiek a plazmy za hyperkoaguláciu, ktorá nezodpovedá gestačnému veku a ako podklad pre vývoj DIC.
V druhom trimestri tehotenstva sa pozorovali zmeny v plazmatickom spojení hemostázy napriek liečbe. Zistilo sa, že APTTV je 10% a AVR je o 5% kratší ako počas fyziologického tehotenstva. Tieto údaje naznačujú zvýšenie hyperkoagulácie. Rovnaký trend bol pozorovaný u trombotického elastogramu: chronometrické koagulácie r + k, parametre Ma a hodnota ITP sú vyššie ako počas fyziologického tehotenstva.
Pri hemostáze krvných doštičiek sa pozoruje štatisticky významné zvýšenie agregácie a zvýšenie hyperfunkčných typov kriviek pri vystavení slabým stimulantom, čo naznačuje pretrvávajúcu hyperaktivitu krvných doštičiek u tehotných žien s APS rezistentnými na liečbu.
V treťom trimestri gravidity sa zaznamenala rovnaká tendencia k zvýšeniu javov hyperkoagulácie napriek pokračujúcej liečbe. Ukazovatele koncentrácie fibrinogénu, AVR a APTT naznačujú vývoj hyperkoagulácie. Hoci kvôli veľkej kontrole hemostasiogramov môžu terapeutické opatrenia udržať hyperkoaguláciu v medziach blízkych fyziologickým parametrom.
Vzhľadom na to, že hlavné, prirodzené inhibítory krvnej zrážanlivosti sú syntetizované vaskulárnou stenou vrátane placentárnych ciev, je veľký záujem vyhodnotiť celkovú aktivitu inhibítora aktivátora plazminogénu (PAI), pretože gravidita prebieha u žien s antifosfolipidovým syndrómom. V dynamike gravidity bolo stanovenie obsahu PAI ukázané, že u gravidných žien s antifosfolipidovým syndrómom nie je zvýšený blokujúci účinok PAI 1 a placentárneho PAI 2.
Maximálny nárast inhibítora aktivátora plazminogénu v jednotlivých pozorovaniach bol 9,2 až 9,7 U / ml (zvyčajne je tento ukazovateľ 0,3 - 3,5 U / ml) na pozadí pomerne vysokej aktivity a obsah plazminogénu - hlavného fibrinolytického substrátu (112 -115% a 15,3-16,3 g / l, s normou 75-150% a 8 g / l. Včasné príznaky patologickej aktivity hemostatického systému (trombínie) v prvom trimestri z hľadiska úrovne inaktívneho antitrombínového komplexu III (TAT) boli zaznamenané iba v jednotlivých prípadoch, čo potvrdzuje skutočnú intravaskulárnu tvorbu prokoagulačnej aktivity.
Štúdie zložiek antikoagulačných mechanizmov systému hemostázy umožnili stanoviť veľkú variabilitu obsahu proteínu C (PrS), vo väčšine prípadov pokles jeho hladiny nezávisí od trvania tehotenstva. Maximálna aktivita ProS nepresiahne 97%, vo väčšine pozorovaní - 53-78% (norma je 70-140%).
Individuálne analýza obsahu inhibítora aktivátora plazminogénu II trimester odhalila dramatický nárast inhibítor plasminogenového aktivátora a 75 U / ml len v jednom prípade bolo zvýšenie kombinácie inhibítora aktivátora plazminogénu s ťažkou patológiou AT III, aktivita 45,5%, koncentrácia 0,423 g / l. Vo všetkých ostatných prípadoch bol obsah inhibítora aktivátora plazminogénu v rozmedzí 0,6 až 12,7 U / ml, v priemere 4,7 ± 0,08 U / ml. Ďalej v treťom trimestri bol obsah inhibítora aktivátora plazminogénu aj naďalej nízky, fluktuácie sa pohybovali v rozmedzí od 0,8 do 10,7 U / ml, v priemere 3,2 ± 0,04 U / ml, iba v jednom pozorovaní - 16,6 U / ml. Vzhľadom k tomu, že obvykle prudký nárast obsahu inhibítora aktivátora plazminogénu znižuje fibrinolytickú aktivitu a miestne trombózy (v dôsledku potlačenia reparačným fibrinolýzy) označené skutočnosti môžeme považovať za nedostatok endoteliálnych odpovedí u tehotných žien s APS, zameraný na syntézu endoteliálny zložky PAI 1 syntetizovanej endotelu cievnej steny a čo je dôležitejšie, absencia systému placentárnej zložky PAI 2 produkovanej placentárnymi nádobami. Možným vysvetlením faktorov, ktoré sme zaznamenali, môže byť narušená funkcia endotelových buniek a predovšetkým placentárne cievy u tehotných žien s antifosfolipidovým syndrómom pravdepodobne v dôsledku fixácie komplexov antigén-protilátka na endotel.
Je pozoruhodné, že významné zníženie aktivity Proc v druhom trimestri tehotenstva je o 29% nižšie ako v kontrolnej skupine.
Vyhodnotenie fibrinolytického systému ukázalo nasledujúce výsledky: vo väčšine pozorovaní bola aktivita plazminogénu vysoká v prvom trimestri 102 ± 6,4% a koncentrácia 15,7 ± 0,0 Eg / l; v druhom trimestri bola aktivita plazminogénu vystavená ešte väčším výkyvom od 112 do 277% a koncentrácia od 11,7 g / l do 25,3 g / l, v priemere 136,8 ± 11,2%, koncentrácia 14,5 ± 0,11 g / l. V treťom trimestri zostali podobné stavy: aktivita plazminogénu bola v rozmedzí od 104 do 234% (norma bola 126,8 ± 9,9%), koncentrácia bola od 10,8 do 16,3 g / l, v priemere 14,5 ± 0,11 g / l , Fibrinolytický potenciál u gravidných žien s antifosfolipidovým syndrómom je teda dosť vysoký.
Na rozdiel od toho bol obsah hlavného inhibítora fibrinolýzy alfa2-makroglobulínu (alfa 2Md) v prvom trimestri gravidity pomerne vysoký, pohyboval sa v rozmedzí od 3,2 do 6,2 g / l (zvyčajne 2,4 g / l), v priemere 3,36 ± 0,08 g / l; v druhom trimestri od 2,9 do 6,2 g / l, v priemere 3,82 ± 0,14 g / l.
Podobné údaje boli získané v súvislosti s obsahom alfa1-antitrypsínu (alfa-ALAT), ktorý sa pohyboval v priebehu všetkých trimestrov tehotenstva od 2,0 do 7,9 g / l. Vzhľadom k tomu, inhibítory CL-Mg a a1-AT je pufrovaný a oneskorené nepriamej akcie, ich vplyv na aktiváciu fibrinolytického systému, a to aj za podmienok vysokého obsahu plazminogénu zjavného zníženia fibrinolytickej kapacity u tehotných žien s antifosfolipidovým syndrómom sú podobné tým, ktoré vo fyziologickom tehotenstva.
Uvedené vlastnosti systému hemostázy zdôrazňujú veľký význam kontrolných štúdií hemostázy počas gravidity na optimalizáciu antitrombotickej liečby a prevenciu iatrogénnych komplikácií.
Štúdia hemostatického systému pred pôrodom ukázala, že hemostatický potenciál zostáva nedotknutý a napriek protidoštičkovej terapii existuje tendencia k hypertrofii krvných doštičiek.
Vzhľadom k tomu, že pacienti s antifosfolipidové syndróm v tehotenstve sú antitrombotiká, a po narodení má vysoké riziko komplikácií trombembolicheskih inherentnú u pacientov s antifosfolipidové syndróm, nesmierne dôležitá je štúdium zastavenie krvácania v popôrodnom období.
Podhodnotenie hemostasiogramu, ukončenie liečby ihneď po podaní môže viesť k rýchlemu rozvoju hyperkoagulácie a tromboembolických komplikácií. Výskum ukázal, že potenciál pre zrážanie krvi zostáva vysoký aj po pôrode, dokonca aj v prípadoch, keď pacienti dostali heparínovú terapiu. Štúdie systému hemostázy by sa mali uskutočňovať 1, 3 a 5 dní po narodení. Mierna hyperkoagulácia bola zaznamenaná u 49% puerperov a u 51% puerperov sa zaznamenala aktivácia systému hemostázy - zvýšenie hyperkoagulácie a výskyt PDF.
Vrodené chyby hemostázy
V súčasnej dobe sa veľa pozornosti venuje geneticky určeným formám trombofílie, ktoré sú rovnako ako antifosfolipidový syndróm sprevádzané tromboembolickými komplikáciami počas tehotenstva a v ktorejkoľvek fáze vedú k strate tehotenstva. Hlavné príčiny dedičné trombofília: antitrombínu deficitu, proteínu C a S, heparínového kofaktora H, nedostatku faktora XII, a pohybu gipoplazminogenemiya, disfibrinogenemiya, deficite aktivátora tkanivového plazminogénu, Leydenovskaya V génovej mutácie faktora zrážavosti.
Okrem týchto porušení v posledných rokoch pripísať dedičné trombofilná stavy hyperhomocysteinémia - stav, v ktorom v dôsledku dedičné chyby enzýmu methylentetrahydrofolátu reduktázy sú ohrození žilových a arteriálnych trombóz, a v tejto súvislosti - s možnou stratou tehotenstva ranom vývoji eklampsia. Treba poznamenať, že v jednej z posledných publikácií bolo zistené, že hyperhomocysteinémia bola zistená u 11% populácie Európanov. Na rozdiel od iných dedičných hemostázových defektov táto patológia vykazuje už v prvom trimestri začiatky tehotenských strát. Pre hyperhomocysteinémiu je kyselina listová veľmi účinná prevencia trombózy.
Pri identifikácii tehotných žien s dedičnou trombofíliou je potrebné veľmi dôkladné posúdenie údajov o rodinnej anamnéze. Ak máte v tehotenstve blízkych príbuzných tromboembolických komplikácií v mladom veku, ak používate hormonálnu liečbu vrátane perorálnej antikoncepcie, mali by ste sa vyšetriť na dedičné defekty hemostázy, pri ktorých je riziko tromboembolických komplikácií extrémne vysoké.
Antitrombín inaktivuje trombín, faktory IXa, Xa, XIa a CPA. Nedostatok alfa1-antitrombínu je vysoko trombogénny a poskytuje až 50% prípadov trombózy počas tehotenstva. Vzhľadom na heterogenitu porušenia sa frekvencia výskytu tejto chyby pohybuje od 1: 600 do 1: 5000.
Proteín C inaktivuje faktory Va a VIIIa. Proteín S pôsobí ako kofaktor proteínu C a zvyšuje jeho účinok. Nedostatok proteínov C a S sa vyskytuje s frekvenciou 1: 500. Proteín C sa počas tehotenstva prakticky nezmenil, proteín S klesol v druhej polovici tehotenstva a vráti sa do normálu krátko po pôrode. Preto ak sa stanovenie proteínu S bude vykonávať počas tehotenstva, môžu sa získať falošné pozitíva.
V posledných rokoch existuje veľa publikácií o trombofílií spôsobených mutáciami génu faktora V, čo je takzvaná Leidenova mutácia. V dôsledku tejto mutácie proteín C neovplyvňuje faktor V, čo vedie k trombofílii. Táto patológia sa nachádza v 9% európskej populácie. Táto mutácia musí byť potvrdená testovaním DNA pre faktor V Leiden. Frekvencia výskytu mutácie Leiden sa značne líši. Podľa švédskych výskumníkov bol výskyt tejto chyby hemostázy u gravidných žien s trombózou 46 až 60%, zatiaľ čo v Anglicku to bolo iba 14% av Škótsku 8%.

PATHOFYSIOLÓGIA SYSTÉMU HEMOSTÁZY
Hodnota hemostatického systému
1. uchovanie krvi v kvapalnom stave (primeraný pomer aktivity koagulačných a antikoagulačných systémov)
2. Zabráňte a zastavte krvácanie (udržiavanie konštantného objemu krvi v obehu)

TYPY HEMOSTÁZY
cievne doštičiek
(Počiatočné)
- ZASTAVENIE BLEEDING V MICRO SHIPS
koagulačné
(Sekundárne)
FORMÁCIA OBSAHU FIBRÍN

KOMPONENTY SYSTÉMU HEMOSTÁZY
* VASKULÁRNA STEN
* krvné doštičky (monocyty, erytrocyty)
* PLASMOVÉ SYSTÉMY:
- PROKOAGULYANTY
- antikoagulanciá
- FIBRINOLYTIC
- KALLIKREIN-KININOVAYA

KLASIFIKÁCIA HEMOSTASOVÝCH PORÚCH
PRE ETIOLÓGIU
- HEREDITÁRNY
- AKQUIRED
PRE ROZVOJOVÝ MECHANIZMUS
- VASKULÁRNE PORUCHY
hemostáza
- ZLYHANIE COAGULATÓRNEJ HEMOSTÁZY
PRE SMERU ZMIEN
- HYPOCOAGULÁCIA
- HYPERKAGULÁCIA

gipokoagulyatsii
Znížená schopnosť krvných zrazenín s tendenciou k opätovnému krvácaniu a krvácaniu (spontánne alebo po malých úrazoch)

etiológie
1. TROMBOCYTOPIA
2. trombocytopatia
3. VASOPATHY
4. KOAGULOPATIA

trombocytopénia
Patologický stav charakterizovaný znížením počtu krvných doštičiek. (menej ako 150.109 / l)

HEREDITÁRNA TROMBOCYTOPÉNIA
Spravidla je súčasne sprevádzané abnormálnymi defektami doštičiek

ZÍSKANÁ TROMBOCYTOPÉNIA (KLASIFIKÁCIA V RÁMCI ROZVOJOVÉHO MECHANIZMU)
POŠKODENIE PLATELETOV
- imunitné komplexy
- mechanická trauma (splenomegália, hemangióm)
UPLOčENÉ TROMBOCYTOVÉ VZDELÁVANIE
(aplastická anémia, chemické a radiačné poškodenie červenej kostnej drene, náhrada hematopoetického tkaniva nádorom)
ZVÝŠENÉ POUŽITIE PLATELETOV
(trombóza, DIC)

Imúnna trombocytopénia
GETEROIMMUNNAYA
* Vyskytuje sa častejšie v deti
** dôvod - zmeny v antigénnej štruktúre krvných doštičiek (počas poklesu rubeoly, kiahní, adenovírusových vírusov, haptínov získaných z liečiv - chinidínu, sulfónamidov, rifampicínu, vakcín)
***Priaznivý kurz (ak je príčina odstránená, dôjde k úplnej regenerácii)

Imúnna trombocytopénia
autoimunitné
Vyskytuje sa častejšie dospelí
dôvod - nedostatok imunitnej tolerancie voči antigénom vlastných krvných doštičiek
Provokatívne faktory: drogy, vírusy, baktérie

Autoimunitná trombocytopénia
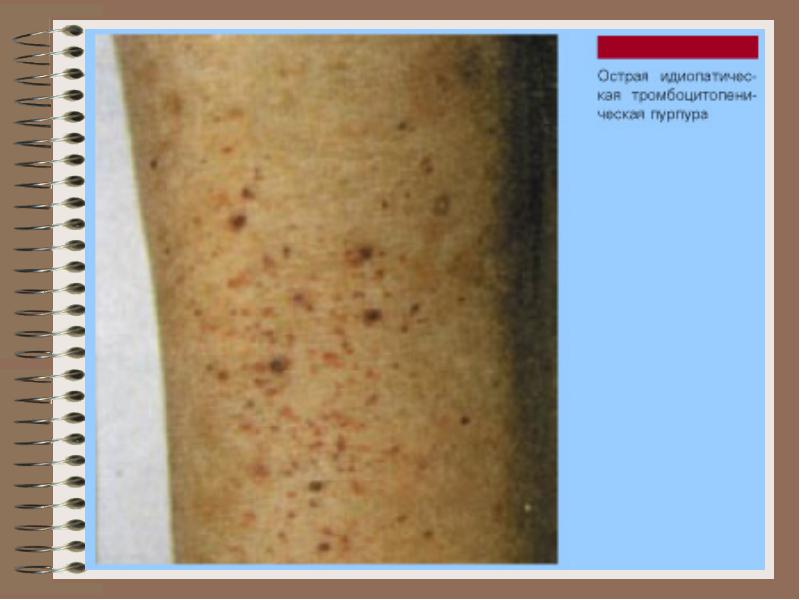
VERLEHOPNÁ CHOROBA
(autoimunitná chronická trombocytopenická purpura)
* Na počítanie povrchu trombocytov IgG zvyšuje sa 10-krát
* Hlavným miestom syntézy IgG je slezina
* Princip liečby:
- splenektómia
- kortikosteroidy
- imunosupresíva
* Neexistuje úplná liečba.

thrombocytopathy
Abnormálna hemostáza v dôsledku kvalitatívnej inferiority alebo dysfunkcie krvných doštičiek, ktorá je charakterizovaná porušením hemostázy krvných doštičiek, výskytom krvácania z tkanív a orgánov

BEZ PORUŠENIA REAKCIE GRANULOVEJ LIBERÁCIE
Glantsman trombasténia
* Dedičstvo - autozomálne recesívne
*dôvod - neprítomnosť glykoproteínov 2b a 3a v plášti krvných doštičiek
*patogenézy- krvné doštičky neovplyvňujú fibrinogén a neagregujú
*príznaky: petechie, krvácanie z nosa, krvácanie z maternice ( môže byť smrteľné!)

Dedičná trombocytopatia
S PORUŠENÍM REAKCIE LIBERÁCIE GRANULOV
dedičstvo - autozomálne recesívne
dôvod - znížená aktivita cykloxygenázy, nízka aktivita kontraktilných proteínov
patogenézy - nedostatok agregácie v interakcii s kolagénom, nedostatok uvoľňovania granúl
príznaky:

Dedičná trombocytopatia
S PORUŠENÍM A UVOĽNENÍM OBSAHU GRANULOV
Choroba Herjman Pudlak (AR)
* dôvod - porušenie hromadenia hustých granúl (ADP, adrenalín, serotonín, Ca2 +),
* patogenézy - v interakcii s kolagénom nedochádza k agregácii, nedochádza k uvoľneniu obsahu granúl
* príznaky: petechie, krvácanie z nosa, krvácanie z maternice

Dedičná trombocytopatia
S DÔSLEDKOM ZLÚČENIA PRÍSLUŠENSTVA A ZLÚČENIA
Von Willebrand-Jurgensov syndróm (AR)
dôvod - nedostatok faktora Willebrand
patogenézy - zhoršenie adhézie krvných doštičiek v dôsledku nedostatku faktora 8
Bernard Sulova choroba (AR)
dôvod - nedostatok glykoproteínu 1 na krvných doštičkách
patogenézy - interakcia krvných doštičiek s von Willebrandovým faktorom, f. 5, f. 11
Znaky - krvácanie z kapilár ( najmä počas puberty alebo pri pôrode)

Dedičná trombocytopatia
NEDOSTATOK A ZNÍŽENÁ DOSTUPNOSŤ f.3
Trombocytopatia Bowe a Aries
dôvod - nedostatok f.3 doštičiek
patogenézy - neexistuje žiadna interakcia medzi krvnými doštičkami a prokoagulantmi
príznaky: petechie, krvácanie z nosa, krvácanie z maternice

Dedičná trombocytopatia
Trombocytopatia v kombinácii s inými dedičnými anomáliami
Whiskott-Aldridgeov syndróm
- dôvod - v krvných doštičkách je niekoľko hustých granúl (ADP, serotonín, adrenalín, Ca2 +), alfa granule (beta-tromboglobulín, fibrinogén, fibronektín, rastový faktor)
- patogenézy - Zhoršená adhézia a agregácia trombocytov, narušenie uvoľňovania granúl
- príznaky:hemoragický syndróm nastáva skoro, môže dôjsť k smrteľnému krvácaniu

Získaná trombocytopatia (etiológia)
1. leukémie- niekoľko granúl v krvných doštičkách spôsobených zrýchlenou maturáciou, zníženou adhéziou a agregáciou
2. VyčistiťIg M - poškodenie receptorov imunitnými komplexmi, porušenie interakcie krvných doštičiek s prokoagulantmi (imunitné ochorenia)
3. hypovitaminóza B12 - uvoľnenie granúl narušené
4. Účinky liekov

Liečivá trombocytopatia
* A inhibítory syntézy tromboxánu A2
steroidné protizápalové lieky
- nesteroidné protizápalové lieky (aspirín blokuje agregáciu trombocytov počas 4-6 dní)
* Stimulátory vzdelávania cAMP
-papaverin
- eufylín
-abolické steroidy
* Ca-iónové antagonisty
-verapamil
-korinfar

VAZOPATIYA
Hemoragická diatéza v dôsledku funkčnej a morfologickej inferiority cievnej steny
- vrodené
- získané

HORNOVÁ VASOPATIA
Bol. Randyu-Osler (hemoragická telangiektázia)
Bol. Fabry (difúzny angiokeróm trupu)
Dedičná trombocytopenická mikroangiomatóza

HORNOVÁ VASOPATIA
dôvod - dedičná porucha vývoja spojivového tkaniva, vrátane vaskulárne subendotelium
vlastnosť
- ohniskové cievne riedenie
- rozšírenie lumen mikrovesselov
- malé kolagénové vlákna v subendotóliu
- plavidlá sú ľahko zranené
- slabá priľnavosť a agregácia krvných doštičiek v dôsledku nedostatku kolagénových vlákien
**Znaky - nazálne, pľúcne-bronchiálne a gastrointestinálne krvácanie (sú smrteľné)

ZÍSKANÁ VASOPATÉDA
1. A diopaticheskaya (Kaposiho sarkóm)
- etiológia - neznáma
2. stagnujúci (dermatitída Klotza, dermatitída Favra Rakusho)
- etiológia - chronické zlyhanie srdca, lokálna venózna insuficiencia
3. dystrofné
Steroidná purpura - hyperfunkcia nadobličiek, liečba kortikosteroidmi - inhibujú syntézu kolagénu
Zhoršovanie - nedostatok Vit.S
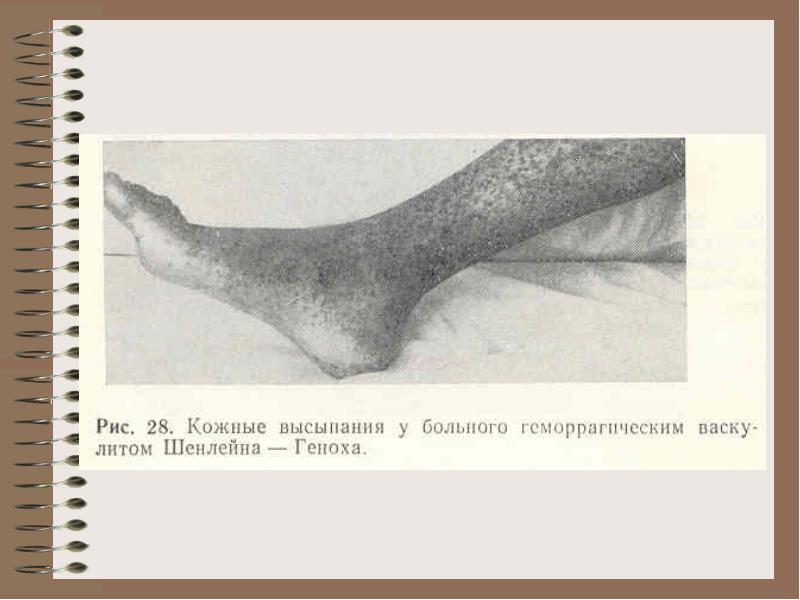
Bol.Shenlein-Genokha - vaskulárne poškodenie imunitných komplexov
4. neurogénna
Klinické príznaky - krvácanie kože

koagulopatie
Hemoragická diatéza, ktorá sa vyskytuje v dôsledku patológie koagulačného systému hemostázy
** dedičný
** získané

Dedičná koagulopatia
Geneticky spôsobená koagulačná porucha spôsobená nedostatkom alebo molekulárnou abnormalitou látok zodpovedných za koagulačnú hemostázu

Dedičná koagulopatia
Klasifikácia
1. Koagulopatia spôsobená izolovaným narušením vnútorného mechanizmu tvorby protrombinázovej aktivity (hemofília A, B, C, Willebrand b., Hagemanova nedostatočnosť)
2. Koagulopatia spôsobená izolovaným porušením externého mechanizmu tvorby protrombinázovej aktivity (hypoprokonvertinémia - nedostatok 7 l)
3. Kombinované porušenie vonkajšieho a vnútorného mechanizmu tvorby protrombinázovej aktivity (parahemofília - nedostatok 5 libier, b.Steuart-Prouer - nedostatok 10 libier)
4. porušenie konečného štádia koagulácie krvi (afibrinogénia)

ŠTATISTIKA
Medzi všetkými formami koagulopatie trpia:
Hemofília A 68 - 78%
B , Willebrand 9 - 18%
Hemofília B 6 - 13%
Hemofília C, parahemofília a hypoprokonvertinémia 1 - 2%
Zostávajúce formy - klinická kazuistika

Hemofília A
Hemoragická diatéza spôsobená dedičnou deficienciou prokoagulačnej časti faktora 8
Faktor 8 (proteín s vysokou molekulovou hmotnosťou)
1. Prokoagulant glykoproteínu (VIII: K)
2. Glykoproteín vykonávajúci adhéziu krvných doštičiek (VIII: FV)
3. Glykoproteín aktivujúci adhéziu krvných doštičiek pod vplyvom ristomycínu (VIII: Rkoff)
4. Antigénny marker VIII: K (VIII: K AG)
5. Antigénny marker VIII: Rkof (VIII: Rkof AG)
Aktivita VIII: K a VIII: PV klesá s klesajúcou multimerickou štruktúrou a iba 8 faktormi

Hemofília A
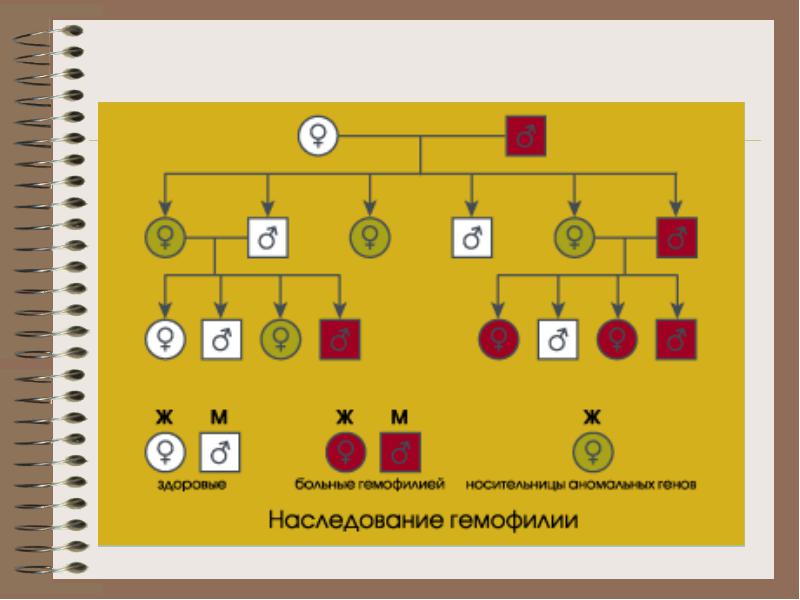
* Uh tiologiya - génová abnormalita v chromozóme X, ktorá riadi syntézu prokoagulačná časť f. 8 (Viii: k)
** III - muži (46, XhY)
** typy
- Syntéza hemofílie A + (antigén-pozitívna forma - anomálna) VIII: K), 8 - 10% trpí
- hemofília A- (antigén-negatívna forma - nie je syntetizovaná VIII: K), Trpí 90-92%
**** poradňa: krvácanie vo veľkých kĺboch, hematómy (subkutánne, intramuskulárne), závažné a dlhotrvajúce post-traumatické krvácanie. Možné krvácanie do brušných orgánov, gastrointestinálne krvácanie

hemofílie
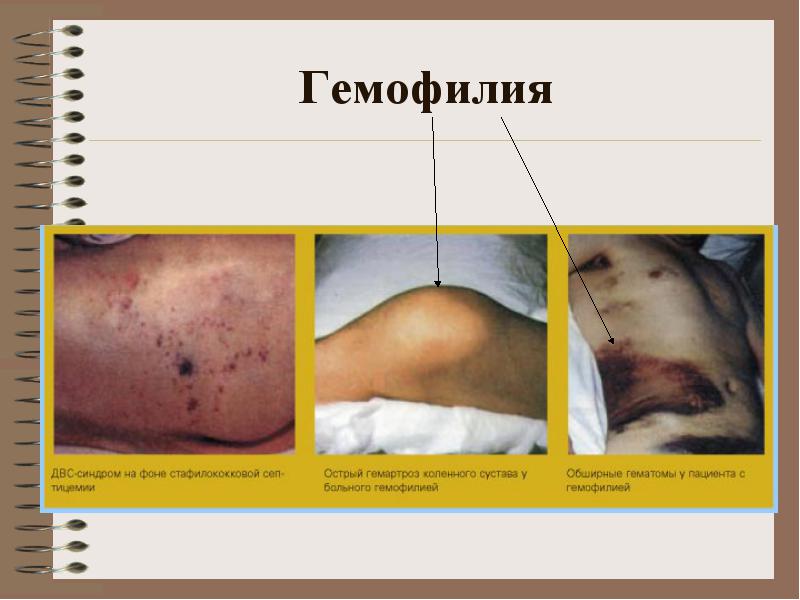
hemofílie
Hemofília B
etiológie - anomália génu v chromozóme X, ktorá riadi syntézu f. 9
Chorí muži (46, XhY)
- ženy (46, XhXh), (45, XhO)
*** Zobrazenie
- Syntéza hemofílie B + (antigén-pozitívna forma - anomálna) f. 9)
- hemofília B- (antigén-negatívna forma - nie je syntetizovaná f. 9)
poradňa: krvácanie vo veľkých kĺboch, hematómy (subkutánne, intramuskulárne), závažné a dlhotrvajúce post-traumatické krvácanie. Možné krvácanie do brušných orgánov, gastrointestinálne krvácanie

POKRAČOVANÁ KOAGULOPATIA
vlastnosť - polydeficient
etiológie
1. Imunná inhibícia prokoagulantov (konflikt rhesus)
2. Nedostatok vit. K-koagulačné faktory (7, 10, 9, 2)
a) narušená syntéza v črevách (dysbakterióza, hnačka)
b) porušenie absorpcie vit. K (nedostatok žlče)
c) závažné poškodenie pečene
3. Predávkovanie heparínom

hyper koaguláciu
ZVÝŠENÁ KAPACITA KREVY VYTVÁRANIE BUNCH V PLAVIDLÁCH
trombóza
DIC

DIC-SYNDRÓM (SYNDRÓM ROZSIABENEJ INTRAVASKULÁRNEJ KOAGULÁCIE V KRVI)
Klasifikácia
* Podľa klinického kurzu
1) akútne (okamžité formy sú charakterizované ťažkým priebehom)
2) chronické
* Podľa prevalencie
1) lokalizované
2) všeobecné

etiológie
Infekcie, septické stavy
otras (s mierou septického úhynu 100%)
Chirurgické intervencie, popáleniny
Všetky podmienky terminálu, zastavenie srdca
Akútna intravaskulárna hemolýza
Pôrodná porucha (20-25%)
Hemoblastóza (s leukémiou - 33-45%)
Deštruktívne procesy v parenchýmových orgánoch
Alergické reakcie

Etapy DIC
1) Hyperkoagulácia (tvorba viacerých krvných zrazenín v dôsledku aktivácie koagulačného systému)
2) konzumná koagulopatia (vyčerpanie koagulačného systému, nadmerné používanie krvných doštičiek na tvorbu krvných zrazenín)
3) Hypokoagulácia (zníženie aktivity koagulantov, aktivácia antikoagulancií, aktivácia fibrinolýzy)
4) Dokončenie (zotavenie, komplikácie, smrť)

Patogenéza DIC
1) hyperthrombinemia (tromboplastín vstupuje do krvi vo veľkom množstve z poškodených tkanív a podporuje tvorbu trombínu). Pri infekciách aktivované makrofágy monocytov syntetizujú svoje vlastné koagulanty (f.7, f.10, f.9, f.2)

Patogenéza DIC
2) Masívna agregácia doštičiek (spôsobuje vývoj konzumácie trombocytopénie a komplikuje krvácanie)
3) Trauma a hemolýza erytrocytov (produkuje veľa ADP, čo zvyšuje adhéziu a agregáciu krvných doštičiek)

Patogenéza DIC
4) "Výbuch humorálnej proteázy" (pri aktivácii prokoagulantov, antikoagulantov, fibrinolytických látok, proteínov systému kalikreín-kinín, systém komplementu v krvi nahromadzuje mnohé produkty rozkladu bielkovín, ktoré sú veľmi toxické a poškodzujú cievy a tkanivá)

Patogenéza DIC
5) Vyčerpanie systému prenájmu fibrín
(prispieva k trombóze)
6) Vyčerpanie koagulačných faktorov krvi
(spôsobuje vznik krvácania)

Klinika DIC
1. Hemokoagulačný šok
dôvod
* porušenie mikrocirkulácie (spôsobuje vývoj hypoxie tkaniva)
* akumulácia toxických produktov proteolýzy
prejavy
* zníženie krvného tlaku
* zníženie centrálneho venózneho tlaku
* krvácanie (vyvolanie hemoragického šoku)

Klinika DIC
2. Hemostatické poruchy
a) hyperkoagulácia
Hlavným prejavom je trombóza.
Krv koaguluje in vitro
b) hypocoagulation
Hlavným prejavom je krvácanie
(zároveň je vyčerpaný systém fibrinolýzy)

Klinika DIC
3. trombocytopénia
Vyskytuje sa v dôsledku tvorby veľkého množstva krvných zrazenín v cievach (konzumácia trombocytopénie)

Dievča po bolestiach v krku vyvinulo petechiálnu vyrážku na kožu končatín a tela. Objektívne: počet krvných doštičiek je 80 g / l, protilátky proti krvným doštičkám. Alergické reakcie typu (podľa Coombsovej a Jelovej) sú základom tejto choroby?
Typ II (humorálna cytotoxicita)
Typ I (anafylaktický)
Typ III (imunokomplex)
Typ V (Stimulácia)
Zhoršená adhézia krvných doštičiek k kolagénu pacienta a pozorovanie krvácania z malých ciev. Porušenie hemostázy spojenia, ktoré možno tolerovať u pacienta?
@Vaskulárne krvné doštičky
Koagulácia a fáza
Koagulačná fáza III
fibrinolýza
Koagulácia, II fáza
Pacientovi je diagnostikovaná trombocytopénia. Aké klinické prejavy sú typické pre poruchy hemostázy krvných doštičiek?
@ Petechia, ekchymóza (modrina)
hemarthrosises
hematóm
Znížená doba krvácania
Zvýšená doba zrážania krvi
Počas vyšetrenia pacient zistil trombocytopatiu. Uveďte, ktorá zmena hrá dôležitú úlohu v patogenéze trombocytopatie?
Výroba patologických krvných doštičiek kostnou dreňou
Znížená antikoagulačná aktivita
Hyperaktivácia trombocytopoézy
Zvýšená koncentrácia prokoagulantov v krvi
Inhibícia fibrinolýzy.
Pred chirurgickým zákrokom sa zistilo, že u ľudí sa čas krvácania zvýšil na 10 minút. Aký nedostatok vytvorených prvkov v krvi môže spôsobiť takéto zmeny?
@ Počet krvných doštičiek
Červené krvinky
monocyty
lymfocyty
Počet bielych krviniek
U pacientov predĺžené užívanie aspirínu spôsobilo krvácanie. Cieľ: trombocytopénia s poruchou funkčnej aktivity krvných doštičiek. Trombocytopatia je v tomto prípade spôsobená inhibíciou aktivity:
@ Cyklo-oxygenázy
Cytochrózooxidáza
lipoxygenázy
Superoxid dismutáza
Fosfolipáza A2.
Pacientovi bola diagnostikovaná znížená produkcia vaskulárneho endotelu ciev von Willebrandovej. Čo je to porušenie hemostázy cievnych krvných doštičiek pozorované v tomto prípade?
Porušenie adhézie krvných doštičiek
Porucha agregácie krvných doštičiek
hyper koaguláciu
Porušenie fibrínovej polymerizácie
Posilnenie fibrinolýzy
Dieťa s hemoragickým vyrážkou, ktoré sa objavilo po akútnej respiračnej vírusovej infekcii, bolo diagnostikované s hemoragickou vaskulitídou (Shenlein-Henochova choroba). Alergické reakcie typu (podľa Coombsovej a Jelovej) sú základom tejto choroby?
Typ III (imunokomplex)
Typ I (anafylaktický)
Typ II (humorálna cytotoxicita)
Typ IV (bunková cytotoxicita)
Typ V (Stimulácia)
Dieťa s hemoragickým vyrážkou, ktoré sa objavilo po akútnej respiračnej vírusovej infekcii, bolo diagnostikované s hemoragickou vaskulitídou (Shenlein-Henochova choroba). Čo spôsobuje zhoršenú hemostázu v tejto chorobe?
Poškodenie cievnej steny
Dedičná porucha spojivového tkaniva cievnej steny
Dedičný nedostatok antikoagulancií
Inhibícia fibrinolýzy
Dedičná prokoagulačná deficiencia
Žena, ktorá trpí ochorením žlčových kameňov, má hemoragický syndróm v dôsledku nedostatku vitamínu K. Ktorý z nasledujúcich faktorov nie je vhodný pre hypovitaminózu K?
@ Stuart - Prouer (f. X)
Faktor von Willebrandovej
Stabilizácia fibrínu (f XIII)
Fibrinogén (f. I)
Počas vyšetrenia bola pacientovi zistená trombofilia (zrýchlenie zrážania krvi). Čo by mohlo spôsobiť porušenie?
Nedostatok inhibítorov proteolytických enzýmov
Zvýšenie koncentrácie prostacyklínu
Znížená koncentrácia krvného trombínu
Zvýšenie koncentrácie heparínu v krvi
Zvýšenie koncentrácie fibrinolyzínu v krvi
Pacient s ochorením pečene má zníženie množstva protrombínu v krvi. To bude viesť k porušeniu predovšetkým:
Druhá fáza koagulačnej hemostázy
fibrinolýza
Tretia fáza koagulačnej hemostázy
Krvná hemostáza krvných doštičiek
Prvá fáza koagulačnej hemostázy
Chlapec po siedmich rokoch, po páde z bicykla, sa objavil hemartróza kolena. Zavedenie kryoprecipitátu a čerpanie krvi z kĺbu viedlo k výraznému zlepšeniu stavu dieťaťa. O akej chorobe by som mal myslieť?
@Hemophilia A
Hemoragická vaskulitída.
thrombocytopathy
trombocytopénia
Reumatoidná artritída
Chlapec s výrazným hemoragickým syndrómom v krvnej plazme chýba antihemofília globulín A (faktor VIII). Aká je primárna fáza hemostázy u tohto dieťaťa?
@ Vnútorná dráha aktivácie protrombinázy
Zrážanie krvných zrazenín
Externá aktivácia protrombinázy
Chlapec trpí hemofíliou. Aké klinické príznaky poškodenia koagulačnej hemostázy?
Petechiálne krvácanie
mikrohematúriou
Ekchymóza (modrina)
Zhoršenie zraku
@ Hematómy, dlhotrvajúce krvácanie
Obeť nehody po nejakom čase po utrpení polytrauma vyvinula rozptýlený intravaskulárny koagulačný syndróm (DIC). Aký faktor bol iniciátorom tejto komplikácie?
Tkanivový tromboplastín (III)
Fibrinogén (f. I)
Antihemofilný globulín A (f VIII)
Pacient s akútnou pankreatitídou vyvinul diseminovaný intravaskulárny koagulačný syndróm (DIC). Aká látka bola iniciátorom tejto komplikácie?
@ Trypsín
Fibrinogén (f. I)
Antihemofilný globulín A (f VIII)
Stuart Factor - Prauera (f. X)
Antihemofilný globulín B (f IX)
U pacientov s polytraumou a akútnym renálnym zlyhaním bol stav komplikovaný vnútorným krvácaním. Aké je hlavné spojenie v patogenéze tejto fázy DIC?
· Spotreba faktorov koagulácie krvi
Uvoľňovanie leukocytov z depa
thrombocytosis
Aktivácia protrombinázy
Inhibícia fibrinolýzy
Pacient s horúčkovým ochorením vyvinul ako komplikáciu DIC syndróm. Ktorému štádiu syndrómu DIC možno podozrievať, ak je známe, že krv pacienta koaguluje za menej ako 3 minúty?
@ Hyper koaguláciu
gipokoagulyatsii
zotavenie
latentne
terminál
Pacient so zranením vyvinul DIC - syndróm. Aké zmeny v hemostáze sú pozorované v druhej fáze syndrómu DIC?
@ Hypocoagulation
Hyperkoagulácia.
fibrinolýza
trombocytopénia
thrombocytopathy
Pacient po transfúzii nezlučiteľnej krvi mal DIC - syndróm. Aké je hlavné spojenie v patogenéze tejto komplikácie pri hemolýze?
@ Zadanie krvných intracelulárnych proteáz
Akumulácia bilirubínu v krvi
Prebytok krvného tromboplastínu
Nadbytok protrombínu v krvi
Zvýšenie obsahu plazminogénu
Pacient s chronickým zlyhaním obličiek vyvinul DIC. Skúmaním sa zistilo zvýšenie času zrážania krvi, trombocytopénia, zvýšenie hladín komplexov fibrín - monomér a produktov degradácie fibrínu. V akej fáze syndrómu MKe by som mal premýšľať?
@ gipokoagulyatsii
hyper koaguláciu
zotavenie
latentne
nestály
Pacient s chronickou lymfocytovou leukémiou vyvinul krvácanie ako výsledok vývoja syndrómu DIC. Aké zmeny v periférnej krvi budú pozorované?
@ Hipokoagulácia, trombocytopénia
Erytrocytóza, zvýšená viskozita krvi
Trombocytóza, znížená doba zrážania krvi
Hyperkoagulácia, zvýšená agregácia doštičiek
Prokoagulanty zvyšujú aktivitu
Žena so sepsou vyvinula petechiálne krvácanie, znížil počet krvných doštičiek a hladiny fibrinogénu v krvi a objavili sa produkty degradácie fibrínu. Aká by mohla byť príčina výrazných zmien?
@ DIC syndróm
leukopénia
lymfopénia
thrombocytosis
