Підвищений гемостаз. Повного одужання не буває. Всі термінальні стани, зупинка серця

У хворого на цингу спостерігаються кровоточивість ясен і петехії на шкірі. Що викликає порушення гемостазу при цьому захворюванні?
A. @ Порушення синтезу колагену
B. Тромбоцитопенія
C. Надлишок антикоагулянтів
D. Активація фібринолізу
E. Дефіцит прокоагулянтов
У хлопчика з геморагічним синдромом в крові відсутній антигемофільний глобулін А (фактор VIII). Недостатність якого механізму гемокоагуляції має місце у цього хворого?
@ Внутрішній механізм формування протромбінази
Перетворення фібриногену в фібрин
Зовнішній механізм формування протромбінази
Перетворення протромбіну в тромбін
Ретракция кров'яного згустку
Чоловік який протягом двох років хворіє на хронічний мієлоїдний лейкоз, поступив до лікарні у стані гострої ниркової недостатності. Що може бути причиною гострої ниркової недостатності у цього хворого?
@ ДВС - синдром
лімфопенія
нейтропенія
тромбоцитопенія
Недостатня активність яких факторів згортання крові обумовлює розвиток геморагічного синдрому у хворих гіповітамінозом К?
@ X, IX, VII, II
фактор Віллебранда
У пацієнтки, яка систематично вживає ацетилсаліцилову кислоту, з'явилося крововилив. Зі зменшенням активності яких ферментів тромбоцитів пов'язаний розвиток тромбоцитопатии в даному випадку?
@ Циклооксигенази
ліпооксигенази
пероксидази
цитохромоксидази
Глюкозо-6-фосфатдегідрогенази
У дівчинки періодично виникають кровотечі з носа, з'являються невеликі геморагічні висипання на шкірі. При обстеженні виявлено: час кровотечі - 10 хвилин, знижена адгезивная здатність тромбоцитів і низька активність ф. VIII (VIII: С). Яке захворювання у дитини?
@ Хвороба Віллебранда
гемофілія А
гемофілія В
спадкова дісфібріногенемія
тромбоцитопенія
Після перенесеної ангіни у дівчинки 5 років спостерігаються петехіальний висип на шкірі тулуба і кінцівок, кровотечі з ясен. При обстеженні виявлено зменшення кількості тромбоцитів в крові. При якому рівні тромбоцитопенії (Г / л) з'являються її клінічні ознаки?
Що може бути головною ланкою в патогенезі тромбофилии в пацієнтки, яка страждає тромбофлебітом вен нижніх кінцівок?
@ Недостатність антикоагулянтів
тромбоцитопенія
тромбоцитопатія
недостатність прокоагулянтов
З метою діагностики якого зсуву в системі гемокоагуляції призначають дослідження рівня продуктів деградації фібрину в крові?
тромбоцитопатія
тромбоцитопенія
вазопатій геморагічна
У хворого діагностовано генетичний дефект мембранного рецептора до фактору Віллебранда - глікопротеїди (ДП) Ib, який відповідає за початковий етап адгезії тромбоцитів до колагену. Як називається ця хвороба?
@ Бернара - Сульє
Віллебранда
Аддісона - Бірмера
Вільсона - Коновалова
Гланцмана - Негелі
У хворого діагностовано спадковий дефект ДП IIb-IIIa - мембранного рецептора, який забезпечує з'єднання фібрину з мембраною тромбоцитів і потрібен для їх агрегації. Про яку хворобу йде мова?
@ Гланцмана - Негелі
Віллебранда
Аддісона - Бірмера
Вільсона - Коновалова
Бернара - Сульє
У дитини з комбінованим імунодефіцитом при обстеженні крові виявлено зменшення адгезії тромбоцитів до колагену, їх агрегації, ослаблення коагуляції крові і ретракції кров'яного згустку. При якому імунодефіциті спостерігаються подібні зміни?
@ Віскотта - Олдріча
швейцарського типу
Ді - Джорджі
Незелофа
У хворої дівчинки діагностовано тромбастенія Гланцманa. Яке порушення в системі гемостазу має місце при цьому?
@ Дісагрегаціонная тромбоцитопатія
абсолютна тромбоцитопенія
Дісадгезівная тромбоцитопатія
дефіцитна тромбоцитопатія
Дісдегрануляціонная тромбоцитопатія
Учасники експедиції, які перебували на півночі, скаржаться на кровоточивість ясен і петехіальні крововиливи на шкірі. З анамнезу відомо - в раціоні не вистачало аскорбінової кислоти, і це призвело до ламкості судинної стінки. Яка це по патогенезу вазопатій?
@ Диспластична
запальна
Метапластична
дистрофічна
імунна
У хворого після тривалої операції на підшлунковій залозі, післяопераційна рана довго кровоточила. За даними коагулограми виявлено суттєве підвищення рівня плазміну. Яка по патогенезу коагулопатия спостерігається в даному випадку?
@ Фібрінопатія
Протромбіназопатія
Тромбопластінопатія
Тромбінопатія
вазопатій
У хворого діагностовано генетичний дефект V фактора, який стає нечутливим до інактивації антітромботічеським комплексом тромбомодулин-протеїн С, що знижує здатність судинної стінки обмежувати утворення фібрину. Яка патологія згортання крові виникне при цій аномалії?
@ тромбофілією
тромбоцитопенія
тромбоцитопатія
геморагічний синдром
Ключові поняття порушення гемостазу:
1. Порушення гемостазу, коагулопатія (Coagulopathia, коагуло- + грец. Patos - страждання, хвороба) - порушення функції системи згортання і протизгортаючої систем крові.
2. Гиперкоагуляционного-тромботическое стан- стан, що супроводжується патологічним процесом посилення згортання крові внаслідок підвищеної агрегації тромбоцитів, активації плазмових і тканинних факторів згортання крові з утворенням тромбоцитарного і фибринового згустків.
3. Гіпокоагуляціонную-геморагічне стан- стан, що супроводжується патологічним процесом зменшення згортання крові внаслідок зниження агрегації тромбоцитів, інактивації плазмових і тканинних факторів згортання крові з виникненням кровоточивості і кровотеч.
4. ДВС-синдром (тромбоцитопенія геморрагическое стан) - синдром дисемінованого внутрішньосудинного згортання крові - типовий патологічний процес порушення гемостазу в результаті послідовно протікають реакцій згортання крові: гіперкоагуляції (освіта дисемінованих тромбів в микроциркуляторной судинної мережі) і гіпокоагуляції (виснаження тромбогенних факторів і посилення фібринолізу), що супроводжуються масивною кровотечею, важким гемокоагуляціонних шоком і гострою дистрофією внутрішніх органів.
При яких захворюваннях виникає порушення гемостазу:Гемостаз - це складний процес, який запобігає або зупиняє витікання крові з просвіту судини, забезпечує виникнення згортка фібрину, необхідного для відновлення цілісності тканини, і, нарешті, видаляє фібрин, коли потреба в ньому відпадає. У цьому процесі беруть участь чотири основних фізіологічних механізму.
За допомогою системи гемостазу кроввиконує свою найважливішу функцію - підтримання рідкого стану крові, що протікає в кровоносних судинах, і згортання крові при порушенні цілісності судинної стінки і, тим самим, припинення кровотечі і збереження обсягу і складу крові. Система гемостазу многокомпонентна. У ній беруть участь тромбоцити і інші клітини крові, судинна стінка, екстраваскулярний тканину, біологічно активні речовини (тромбоцитарно-судинний гемостаз), плазмові, тканинні фактори згортання крові (коагуляційний гемостаз), що знаходяться в тісній взаємодії з протизгортаючої, фібринолітичної і калікреїн-кінінової системами. Порушення будь-якого з цих компонентів веде до патології гемостазу.
Класифікація порушення гемостазу. Патологія гемостазу класифікується за переважного ураження різних його компонентів на порушення тромбоцитарно-судинного гемостазу і коагуляційного гемостазу. За етіології ці порушення можуть бути придбаними і спадковими, а за спрямованістю змін поділятися на зниження згортання крові (гіпокоагуляція) і підвищення згортання крові (гиперкоагуляцию), яке може бути локальним (тромбоз) і генералізований (ДВС-синдром).
Зниження згортання крові
Зниження згортання крові проявляється підвищеною кровоточивістю (геморагічним синдромом) - повторними кровотечами, крововиливами, які виникають як спонтанно, так і при незначних травмах.
Тромбоцитарно-судинний гемостаз порушується при кількісних і якісних змінах тромбоцитів (тромбоцитопеніях і тромбоцитопатій), а також ураженнях судинної стінки.
Тромбоцитопенією називається зменшення вмісту тромбоцитів у крові нижче норми (180-320 Г / л або 180-320x109 / л). Однак спонтанні кровотечі виникають лише при зниженні їх числа менше 30 Г / л. Під тромбоцитопатії розуміють якісну неповноцінність і дисфункцію тромбоцитів при нормальному або зниженому їх вмісті.Причини зниженого згортання крові. Причиною виникнення тромбоцитопенії нерідко є імунні реакції при зміні антигенної структури тромбоцитів під дією вірусів, лікарських препаратів, виробленні антитромбоцитарних автоантитіл (при хронічному лімфолейкозі, ідіопатичною тромбоцитопенії), несумісності тромбоцитарних антигенів матері і плоду. Крім того, тромбоцитопенія розвивається внаслідок ураження мегакариоцитарного паростка кісткового мозку іонізуючою радіацією, хімічними речовинами або витіснення його пухлинними метастазами, лейкозними інфільтратами. Зниження тромбоцітопоеза може бути обумовлено дефіцитом ціанокобаламіну і фолієвої кислоти, спадковим дефектом утворення тромбоцитів (в тому числі при дефіциті тромбоцітопоетінов). Тромбоцитопенія виникає в результаті механічного пошкодження тромбоцитів при спленомегалії, штучних клапанах серця, а також посиленого споживання тромбоцитів при локальному і генерализованном внутрисосудистом згортання крові.
До етіологічних чинників, що викликають Тромбоцитопатія, відносяться дію токсичних речовин і лікарських препаратів (алкоголь, ацетилсаліцилова кислота), іонізуючої радіації, ендогенних метаболітів (при уремії, цирозі печінки); дефіцит ціанокобаламіну, гормональні порушення (гіпотиреоз). Спостерігаються і генетичні дефекти структури мембрани і біохімічного складу тромбоцитів (дефіцит тромбостенина, фактора 3, АТФ, АДФ, Г-6-ФДГ, мембранних рецепторів для факторів V, VIII, XI і ін.).При геморагічних вазопатій ураження судинної стінки, що приводить до порушення тромбоцитарно-судинного гемостазу і кровоточивості, виникає внаслідок підвищення проникності стінки кровоносних судин і її деструкції при порушенні синтезу колагену (при аліментарному дефіциті аскорбінової кислоти, спадкових дефектах синтезу колагену), при дії біологічно активних речовин ( алергія), радіотоксінов (променева хвороба), імунних геморагічних васкулітах, зниженні ангиотрофическая функції тромбоцитів при тромбоцит Відкритий і тромбоцитопатій, руйнуванні судинної стінки лейкозними інфільтратами. Однією з причин кровоточивості є зменшення вироблення ендотелієм судинної стінки фактора Віллебранда - крупномолекулярний компонента VIII фактора згортання-крові (спадкова хвороба Віллебранда). Цей фактор накопичується в тромбоцитах і звільняється при їх дегрануляції.
Він необхідний для нормальної адгезії тромбоцитів до колагену стінки, і без нього не формується тромбоцитарний тромб. Геморагічний синдром спостерігається і при посиленні перекисного окислення мембранних фосфоліпідів, в результаті чого в ендотелії синтезується і секретується надмірну кількість потужних інгібіторів агрегації тромбоцитів - простациклинов. Крім того, до зниження тромбоцитарно-судинного гемостазу призводить порушення нейрогенної і гуморальної регуляції судинного тонусу, зниження якого веде до неможливості закупорки дрібних судин тромбоцитарним тромбом.
Патогенез зниженого згортання крові. Виділяють чотири основних механізми виникнення тромбоцитопеній: зменшення продукції, посилене руйнування, підвищене споживання (тромбоутворення), перерозподіл тромбоцитів.
Порушення гемостазу і розвиток кровоточивості при тромбоцитопенії обумовлено наступними механізмами:
- підвищенням проникності мікросудин для еритроцитів і інших складових частин крові (діапедезних геморрагия) і ламкість судин внаслідок дистрофії стінки при виключенні ангиотрофическая функції тромбоцитів;
- зменшенням адгезивної-агрегационной функції тромбоцитів;
- порушенням реакції звільнення тромбоцитарних факторів згортання крові, АДФ, серотоніну, адреналіну, антігепарінового фактора, наслідком чого є недостатня формування тромбоцитарного тромбу, відсутність спазму судин і уповільнення згортання;
- зменшенням ретракции згустку в результаті зниження активності скорочувального білка тромбоцитів - тромбостенина (фактор 8 тромбоцитів).У патогенезі ТРОМБОЦИТОПАТІЙ можна виділити два основних механізми їх виникнення - продукція патологічних тромбоцитів в кістковому мозку і деструкція тромбоцитів у всіх відділах системи крові. Патогенез порушення тромбоцитарно-судинного гемостазу при тромбоцитопатій такий же, як і при тромбоцитопеніях, так як пов'язаний з виключенням функцій тромбоцитів.
Порушення коагуляційного гемостазу, що приводить до розвитку кровоточивості, може бути викликано наступними факторами:
- придбаним і спадковим зменшенням або збоченням синтезу плазмових і тромбоцитарних факторів згортання крові та компонентів калікреїн-кінінової системи;
- пригніченням або підвищеним споживанням цих факторів;
- збільшенням ендогенних антикоагулянтів;
- активізацією фібринолітичної системи;
- передозуванням антикоагулянтів, фібринолітичних і дефібрінірующего препаратів. Все це лежить в основі порушення однієї з трьох фаз згортання крові і ретракції згустку або ж поєднаного їх зміни.Причинами порушення першої фази згортання крові - утворення тромбопластину - є зниження продукції факторів (IX, X) при патології печінки, утворення антитіл до деяких факторів (VIII, IX) при захворюваннях, у патогенезі яких є аутоімунний компонент (лейкози, колагенози), або ж передозування такого універсального антикоагулянту, як гепарин. Відомі генетичні дефекти синтезу VIII, IX і XI факторів, дефіцит яких лежить в основі розвитку гемофілії (відповідно послідовності цих факторів - гемофілії А, В і С).
Порушення другої фази згортання крові - утворення тромбіну - виникає не тільки при захворюваннях печінки, а й при гіпо- та авітамінозах К, коли теж знижується синтез в печінці факторів II, V, VII, що беруть участь в цій фазі (при механічної жовтяниці, ентериті, великої резекції тонкої кишки, лікарському дисбактеріозі). Можлива поява імунних інгібіторів факторів V, VII (наприклад, при лікуванні стрептоміцину сульфатом), посилене їх виведення нирками, спадковий дефіцит (фактора V при Парагемофілія) або ж інактивація компонентами протизгортаючої системи - антитромбін, гепарином (при анафілактичний шок, передозуванні гепарину).
Геморагічний діатез, пов'язаний з порушенням третьої фази згортання - фази освіти фібрину, виникає при зменшенні синтезу фібриногену в уражених патологічним процесом печінки, легенів або ж в результаті спадкової гіпо, афібріногенеміі і дефіциту фібрінстабілізірующего фактора (фактора XIII). Однак значно частіше порушення третьої фази є наслідком посилення фібринолізу при травмі (операції) легких, матки, підшлункової залози; опіку, шоці. Це обумовлено підвищеним надходженням в кров активаторів профібринолізину (плазміногену) - тканинних, мікробних фібрінокіназ, лейко- і еритроцитарних активаторів, компонентів калікреїн-кінінової системи і системи комплементу комплексів гепарину з фібриногеном, профібринолізином і адреналіном (ці комплекси забезпечують неферментативного фибринолиз, по Б. А . Кудряшову).
Патогенез. Головними ланками в патогенезі геморагічного діатезу, що розвинувся при порушенні будь-якої з фаз згортання крові, є хронічна крововтрата і її наслідки, а також структурні та функціональні зміни в місці крововиливів (в суглобах, внутрішніх органах, Шкірі та інших тканинах).
Підвищення згортання крові
Підвищення згортання крові проявляється локальним (тромбоз) або генералізованим внутрішньосудинним згортанням крові, в основі чого лежить порушення тромбоцитарно-судинного і коагуляційного гемостазу.Гиперкоагуляция може бути обумовлена:
- підвищенням функціональної активності системи згортання крові за рахунок збільшеного - - надходження в кров прокоагулянтов і активаторів згортання крові;
- збільшенням в крові кількості тромбоцитів понад;
- зниженням антитромботических властивостей судинної стінки;
- зменшенням активності антизсідальної системи крові;
- ослабленням фібринолізу.Генерализованное (дисеміноване) внутрішньосудинне згортання крові (ДВС-синдром) - тяжке порушення гемостазу, що виникає при надмірному надходженні в кров прокоагулянтов і активаторів згортання крові, що веде до утворення множинних микротромбов в судинах мікроциркуляторного русла, а потім розвитку гіпокоагуляції, тромбоцитопенії і геморагії в результаті "споживання" факторів системи згортання і підвищення функціональної активності системи протизгортання і фібринолізу крові з подальшим виснаженням всіх т ех систем.
Етіологія. Універсальність і неспецифичность ДВС-синдрому обумовлені різноманіттям причинних факторів його виникнення. До них відносяться перш за все генералізовані інфекції та септичні стани, всі види шоку, травматичні хірургічні операції, акушерська патологія (передчасне відшарування, ручне відділення плаценти), гострий внутрішньосудинний гемоліз, уремія при нирковій недостатності, все термінальні стану.
Патогенез. Головною ланкою в патогенезі генералізованої гіперкоагуляції є порушення балансу між калікреїн-кінінової, згортання, антизсідальної і фібринолітичної системами крові при надходженні в судинне русло великої кількості прокоагулянтов і їх активаторів. Це і призводить до порушення такої важливої функції крові, як збереження її нормального агрегатного стану, в результаті чого в фазу гіперкоагуляції кров в судинах згортається і припиняється її циркуляція з розвитком важких дистрофічних і функціональних порушень в органах і тканинах, нерідко несумісних з життям. В наступну фазу гіпокоагуляції розрідження крові і втрата здатності до згортання і агрегації тромбоцитів викликають кровотечу, яке погано піддається терапевтичної корекції. За позитивного результату настає третя - відновлювальна фаза, при якій відбувається нормалізація гемостазу.
Стан системи гемостазу визначає перебіг і результат вагітності для матері і плоду. В останні роки відзначається значне число публікацій, що вказують на велику роль тромбофіліческіх ускладнень в звичному невиношуванні, внутрішньоутробної загибелі плоду, відшарування плаценти, в розвитку еклампсії, затримки внутрішньоутробного розвитку.
Основні механізми гемостазу
Системою гемостазу або системою регуляції агрегатного стану крові (PACK) називають біологічну систему, яка забезпечує регуляцію агрегационной стану крові і підтримання необхідного для організму гемостатического потенціалу. Система PACK мозаїчна, тобто гемостатический потенціал в різних ділянках кровотоку неоднаковий. Цей стан є нормальним для функціональної системи. У систему регуляції агрегатного стану крові включаються:
- центральні органи системи - кістковий мозок, печінка, селезінка;
- периферичні освіти - огрядні клітини, ендометрій і інші шари судинної стінки, клітини крові;
- місцеві регуляторні системи - вегетативна нервова система, підкіркові структури.
Система гемостазу регулюється складними нейрогуморальними механізмами. Ці механізми створюють умови, при яких почався місцево процес згортання, необхідний для зупинки кровотечі, не переходить при нормальному функціонуванні системи в процес загального внутрішньосудинного згортання.
Виділяють чотири основних ланки в системі гемостазу:
- Судинно-тромбоцитарное ланка;
- прокоагулянти;
- Фібринолітичний ланка;
- Ланка інгібіторів згортання крові.
Судинно-тромбоцитарное ланка
Судинно-тромбоцитарное ланка системи гемостазу нерідко позначають як первинний гемостаз. Ендотелій кровоносних судин відіграє важливу роль у підтримці агрегатного стану циркулюючої крові. Це пов'язано з наступними його особливостями:
- здатністю утворювати і виділяти в кров потужний інгібітор агрегації тромбоцитів - простациклін (метаболіт арахідонової кислоти);
- продукцією тканинного активатора фібринолізу;
- нездатністю до контактної активації системи згортання крові;
- створенням антикоагулянтного потенціалу на кордоні кров / тканина шляхом фіксації на ендотелії комплексу гепарин-антитромбін III;
- здатністю видаляти з кровотоку активовані фактори згортання.
Участь тромбоцитів у гемостазі визначається їх здатністю до адгезії у місця пошкодження ендотелію, процесом їх агрегації і утворення первинної тромбоцитарної пробки, а також їх здатність підтримувати спазм судин шляхом секреції вазоактивних речовин - адреналіну, норадреналіну, серотоніну, АДФ і ін., А також утворювати, накопичувати і секретувати речовини, що стимулюють адгезію і агрегацію.
Таким чином, численні дослідження, дозволили зробити висновок, що первинний гемостаз здійснюється в основному тромбоцитами, а не згортанням крові. Провідна роль в реалізації первинного гемостазу належить адгезивної-агрегационной функції тромбоцитів.
Адгезія - прилипання тромбоцитів до ділянки ушкодження судинної стінки, кколлагеновим волокнам судинної стінки, до мікрофібріну і еластину. Найважливішими плазмовими кофакторами цього процесу є іони кальцію і синтезується в ендотелії білок - фактор Віллебранда і глікопротеїди тромбоцитарной мембрани. Фізіологічна призначення адгезії - закрити дефект судинної стінки. Одночасно з адгезію протікає агрегаціятромбоцитів. При цьому тромбоцити не тільки склеюються між собою, але і прилипають до адгезірованних тромбоцитам, завдяки чому утворюється гемостатическая пробка. З тромбоцитів в процесі адгезії і агрегації активно секректіруются гранули, які містять речовини, що підсилюють процес агрегації і утворюють її другу хвилю. Реакція вивільнення тромбоцитарних факторів - АДФ, адреналіну, норадреналіну, серотоніну, антігепарінового фактора, бета-тромбоглобуліна і ін. Пізніше секретируются гранули, які містять лізосомальніферменти (реакція звільнення II). Вихід адреналіну, норадреналіну і серотоніну не тільки підсилює агрегацію, а й сприяє вторинному спазму кровоносних судин, що супроводжується надійною фіксацією тромбоцитарной пробки у місця пошкодження судини. В результаті взаємодії тромбоцитарний і плазмових факторів в зоні гемостазу утворюється тромбін, який не тільки підсилює агрегацію тромбоцитів, але одночасно є стимулятором згортання крові, що утворюється при цьому фібрин формує тромб, який стає щільним і непроникним для плазми і сироватки, відбувається його ретракція.
Значною мірою механізм агрегації тромбоцитів став зрозумілий після відкриття простагландинів в тромбоцитах і судинної стінки. Різні агрегує агенти активують фосфоліпазу А1, яка викликає відщеплення від фосфоліпідів арахідонової кислоти - потужного агрегує речовини. Під впливом простагландінсінтетази утворюються циклічні ендоперекісі простагландинів, що стимулюють в тромбоцитах скорочення фібрил і надають потужне агрегує дію. Під впливом тромбоксансинтетази в тромбоцитах синтезується тромбоксан А1. Останній сприяє транспорту Са 2+ в тромбоциті, що призводить до утворення АДФ - основного ендогенного стимулятора агрегації. Рівень цАМФ-універсального біологічного переносника регулюється аденилатциклазой, що каталізує реакцію АТФ-цАМФ.
Аналогічний процес відбувається в ендотелії судин - під впливом простагландінсінтетази з арахідонової кислоти утворюються ендоперекісі простагландинів. Далі під впливом простаціклінсінтетази утворюється простациклін (простагландин L), який володіє потужним дезагрегірующім дією і активізує аденілатциклазу.
Таким чином, формується т.зв. тромбоксан - простациклінової баланс - один з основних регуляторів стан тонусу судинної стінки і агрегації тромбоцитів.
Прокоагулянтную ланка гемостазу
У процесі згортання крові беруть участь сполуки, що містяться в плазмі (прокоагулянти). Це складний багатоетапний ферментний процес, який можна умовно розділити на 3 стадії.
- I стадія - комплекс реакцій, що призводять до утворення протромбин активного комплексу або протромбінази. До складу комплексу входять фактор X, третій фактор тромбоцитів (фосфолипид), V фактор і іони Са 2+. Це найбільш складна і тривала фаза.
- II стадія - під впливом протромбінази протромбін переходить в тромбін.
- III стадія - під впливом тромбіну фібриноген переходить в фібрин.
Ключовим моментом утворення протромбінази є активація X чинника згортання крові, що може здійснюватися двома основними механізмами запуску процесу згортання - зовнішнім і внутрішнім.
При зовнішньому механізмі згортання стимулюється надходженням в плазму тканинного тромбоплазміна (III або комплексу фосфолипид-апопротеїн III). Цей механізм визначається тестом протромбінового часу (ПВ).
При внутрішньому механізмі згортання здійснюється без участі тканинного тромбопластину. Пусковим фактором при цьому шляху згортання є активація фактора X. Активація фактора X може відбуватися за рахунок контакту з колагеном при пошкодженні судинної стінки або ферментним шляхом під впливом калікреїну, плазміну чи інших протеаз.
Як при зовнішньому так і при внутрішньому шляху згортання взаємодія і активація факторів здійснюється на фосфоліпідних мембранах, на яких за допомогою іонів Са фіксуються білкові фактори згортання.
Номенклатура плазмових факторів згортання:
- I - фібриноген;
- II - протромбін;
- III - тканинної тромбопластин;
- IV - кальцій;
- V - акселеріруют фактор;
- VI - активатор V фактора;
- VII - проконвертин;
- VIII - антигемофільних глобулін А;
- IX - антигемофільний фактор В (фактор Крістмас);
- X - протромбіназа;
- XI - плазмовий попередник тромбопластину;
- XII - фактор Хагемана;
- XIII - фибриназа.
Зовнішній і внутрішній механізм активації системи згортання крові не ізольовані один від одного. Включення «мостів» між ними служить діагностичним ознакою при розпізнаванні внутрішньосудинної активації системи згортання. При аналізі результатів основних коагуляційних тестів необхідно враховувати наступне:
- З плазмових факторів згортання лише фактор VII бере участь у зовнішньому механізмі згортання, і при його дефіциті подовжується лише протромбіновий час.
- Фактори XII, IX, XI, VIII і прекалікреїн бере участь тільки у внутрішньому механізмі активації, в зв'язку з чим при їх дефіциті порушується АЧТЧ і аутокоагуляціоннийтест, в той час як протромбіновий час залишається нормальним.
- При дефіциті факторів X, V, II, I на яких замикаються обидва механізму згортання, патологія виявляється у всіх перерахованих тестах.
Крім зовнішнього і внутрішнього механізмів гемокоагуляції в організмі є додаткові резервні шляхи активації, які включаються по «вимогу». Найбільш важливим шляхом є макрофагальний - моноцитарний механізм гемокоагуляции. При активації ендотоксинами або іншими інфекційними антигенами ці клітини починають секретувати більшу кількість тканинного тромбопластину.
Ендогенні інгібітори коагуляції
Для підтримки крові в рідкому стані і для обмеження процесу тромбоутворення необхідні фізіологічні антикоагулянти. В даний час відомо, що природні антикоагулянти представляють собою велику групу сполук, що діють на різні фази процесу гемостазу. Більш того багато антикоагулянти одночасно впливають на фібріногенез, генерацію калікреїн-кінінової системи, систему комплементу.
Природні антикоагулянти поділяють на первинні, постійно присутні в плазмі і клітинах крові і діючі незалежно від освіти або розчинення кров'яного згустку, і вторинні, які виникають в процесі згортання крові і фібринолізу, завдяки протеолитическому дії ферменту на субстрат. До 75% природного антикоагулянтної потенціалу припадає на частку антитромбіну III (AT III). Антитромбін III здатний блокувати протромбіназа як за зовнішнім так і за внутрішнім механізмом, тому що, будучи інгібітором факторів XII а, ХIа, IX а, VIII а, калікреїну, A III пов'язує плазмин. Активність антитромбіну III посилюється більш ніж в 100 разів при утворенні комплексів з гепарином. Гепарин поза зв'язком з антитромбіном III не володіє антикоагулянтну дію. При зниженні рівня антитромбіну III виникає важке тромбофіліческіе стан, що характеризується рецидивуючими тромбозами, тромбоемболії легеневої артерії, інфарктами. При зниженні антитромбіну III нижче 30% хворі гинуть від тромбоемболії, причому гепарин не виявляє на їх кров антикоагулянтної дії. Дефіцит антитромбіну III формує гепариніндукованої резистентність.
До природних антикоагулянтів відноситься протеїн С, протеїн S, альфа2-макроглобулин.
Протеїн С - профермент, активується тромбіном і фактором Ха. Активація йде в комплексі з фосфоліпідів і кальцієм. Процес посилюється під впливом тромбомодулина і протеїну S, який послаблює здатність тромбіну активувати фактори VIII і V. При дефіциті протеїну С відзначається схильність до тромбозів, що спостерігається при гострому ДВС-синдромі, респіраторному дистрес-синдромі та ін.
У процесі згортання крові і фібринолізу утворюються вторинні, природні антикоагулянти в результаті подальшої ферментативної деградації факторів згортання.
Патологічні антикоагулянти відсутні в крові в нормальних умовах, але з'являються при різних імунних порушеннях, до них відносяться антитіла до факторів згортання крові, частіше за все до факторів VIII і V (нерідко виникають після пологів і масивних гемотрансфузій і імунні комплекси - вовчаковий антикоагулянт, антитромбін V) .
фибринолитическая система
Фибринолитическая система складається з плазміногену і його активаторів і інгібіторів.
Плазміноген-активатори - група чинників, які перетворюють плазміноген в плазмін. До них відносяться такі речовини какурокіназа, бактеріальні ензими. Активний плазмин швидко блокується антиплазміном і елімінується з кровотоку. Активація фібринолізу, як і активація згортання крові здійснюється як за зовнішнім, так і по внутрішньому шляху.
Внутрішній шлях активації фібринолізу обумовлений тими ж факторами, що і згортання крові, тобто факторами ХIIа або XIII з КАЛІКРЕЇН і кініногенов. Зовнішній шлях активації здійснюється за рахунок синтезованих в ендотелії активаторів тканинного типу. Активатори тканинного типу містяться в багатьох тканинах і рідких середовищах організму, клітинах крові. Відзначено зниження фибринолиз антиплазміном альфа2-глобуліном, альфа2 макроглобуліном, антитрипсин та ін. Плазмінової система адаптована до лізису фібрину в згустках (тромбах) і розчинних фібрин-мономірних комплексах (РФМК). І тільки при надмірній її активації виникає лізис фібрину, фібриногену та інших білків. Активний плазмин викликає послідовне розщеплення фібриногену / фібрину з утворенням продуктів їх деградації (ПДФ), наявність яких свідчить про активацію фібринолізу.
Як правило, в більшості клінічних спостережень активація фібринолізу вторинна і пов'язана з дисемінованого внутрішньосудинного згортанням крові.
У процесі згортання і фібринолізу з'являються вторинні, природні антикоагулянти - ПДФ і інші відпрацьовані фактори згортання крові - біологічно активні, які діють як антиагреганти і антикоагулянти.
В даний час розрізняють імунні тромбофіліческіе ускладнення і спадкові дефекти гемостазу.
Система гемостазу при вагітності
Домінує точка зору, згідно з якою в організмі вагітної жінки створюються певні умови для розвитку синдрому ДВС. Це виражається в підвищенні загального коагулянтной потенціалу (сумарна активність факторів згортання), підвищенні функціональної активності тромбоцитів при деякому зниженні їх кількості, зниження фібринолітичної активності при збільшенні ПДФ, зниження активності антитромбіну III при деякому зменшенні його змісту. Ці особливості носять компенсаторно-пристосувальний характер і необхідні як для нормального формування фетоплацентарного комплексу, так і для обмеження крововтрати під час пологів. В активації системи гемостазу велику роль відіграють зміни загальної гемодинаміки в організмі вагітної жінки. Для нормального функціонування фетоплацентарної системи в умовах високого коагуляционного потенціалу крові вступають в дію компенсаторно-пристосувальні механізми: збільшення кількості термінальних ворсин малого калібру з гіперплазією і периферичних розташуванням капілярів, зменшення товщини плацентарного бар'єру з тонкою синцития, освіту сінцітіокапіллярних мембран, синцитіальних вузликів.
Особливості функціонування системи гемостазу пов'язані з певними змінами в системі спіральних артерій матки. Це - інвазія клітин трофобласта в стінку спіральних артерій, заміщення внутрішньої еластичної мембрани і внутрішньої медії товстим шаром фібрину, порушення цілісності ендотелію і оголення коллагеннових субендотеліальних структур. У цьому процесі має значення і розгортання межворсінчатого простору з властивими йому морфологічними і гемодинамічними особливостями.
Особливості системи гемостазу при фізіологічно протікає вагітності визначаються формуванням матково-плацентарного кола кровообігу.
Рівень тромбоцитів при неускладненому перебігу вагітності залишається практично незмінним, хоча є дослідження, де відзначено зниження рівня тромбоцитів. При зниженні рівня тромбоцитів нижче 150000 / ml необхідні дослідження для виявлення причин розвитку тромбоцитопенії.
При вагітності спостерігається зростання коагулянтной потенціалу, організм як би готується до можливого кровотечі в процесі пологів. Відзначено зростання всіх факторів згортання за винятком фактора XI і XIII.
Збільшення рівня фібриногену починається з 3-го місяця вагітності і незважаючи на збільшення об'єму циркулюючої плазми рівень фібриногену в кінці вагітності збільшується не менш ніж в два рази в порівнянні з невагітним станом.
Активність фактора VIII (фактора Віллебранда) також збільшується і не тільки у здорових жінок, а й у пацієнток - кондукторів гемофілії і хворих на хворобу Віллебранда. Слід враховувати, що при легкій і среднетяжелой ступеня цього захворювання рівень цього фактора може бути практично нормальним. На противагу загального збільшення факторів згортання відзначено при вагітності деяке зниження XI фактора в кінці вагітності і більш помітне зниження XIII фактора (фібрин-стабілізуючого фактора). Фізіологічна роль цих змін поки не ясна.
Коагуляційний потенціал крові зростає ще в зв'язку з тим, що знижується рівень антитромбіну III, протеїн С підвищується в основному в післяпологовому періоді, а протеїн S знижений при вагітності і значно знижений після пологів.
При вагітності відзначено зниження фібринолізу в кінці вагітності і в процесі пологів. У ранньому післяпологовому періоді активність фібринолізу повертається до норми. Щодо присутності в кровотоці ПДФ в літературі є суперечливі дані. За результатами дослідження, відзначено невелике збільшення ПДФ в останні місяці вагітності. За даними досліджень, при неускладненому перебігу вагітності збільшення вмісту продуктів деградації не виявляється аж до початку пологів. За даними J. Rand і співавт. (1991), рівень деяких фрагментів продуктів деградації фібрину підвищується з 16 тижнів вагітності і досягає плато в 36-40 тижнів. Однак значне збільшення ПДФ при вагітності швидше за все є відображенням фибринолитического процесу в зв'язку з активацією внутрішньосудинного згортання.
Зміна системи гемостазу у вагітних з антифосфоліпідним синдромом
Показники системи гемостазу у вагітних з антифосфоліпідним синдромом суттєво відрізняються від показників у жінок з фізіологічним перебігом вагітності. З моменту настання вагітності у більшості пацієнток відзначені зміни тромбоцитарного ланки гемостазу. Агрегаціятромбоцитів при стимуляції АДФ на 55-33% вище, ніж при фізіологічному перебігу вагітності. Тенденція до підвищення агрегації зберігається на тлі антиагрегантної терапії.
Агрегаціятромбоцитів під дією колагену в 1,8 рази вище, ніж при фізіологічному перебігу вагітності. Агрегаціятромбоцитів під дією адреналіну на 39% вище, ніж в групі контролю. Якщо під впливом проведеної терапії не вдається знизити ці показники, то така стійка гіперактивність тромбоцитів є підставою для збільшення дози антиагрегантов або призначення додаткових антиагрегантних засобів. Показники ристомицин - агрегації в середньому в I триместрі залишаються в межах норми. Проведені дослідження показали, що з ранніх строків вагітності у пацієнток з АФС є підвищена реакція тромбоцитів до дії біологічних індукторів, виявлених в основному в тестах функціональної активності тромбоцитів, таких як агрегація під впливом АДФ 1х10 3 М і 1х10 5 М, арахідонової кислотою.
При оцінці якісних характеристик за типами агрегатограмм ні в одному спостереженні не відзначено дезагрегации (оборотної агрегації) при впливі навіть слабких стимулів АДФ 1 х10 7 М. Про це свідчить зміна профілю кривих в сторону так званих «нетипових» гіперфункціонального агрегатограмм.
Показники плазмового ланки гемостазу в I триместрі вагітності також змінені в порівнянні з контролем: відзначено достовірне прискорення АВР, на тромбоеластограмме укорочений показник r + k, достовірно вище показник структурних властивостей фибринового згустку - ІТП.
Таким чином, у вагітних з АФС вже в I триместрі відмічається помірна гіперкоагуляція в плазмовому ланці гемостазу, що розвивається раніше, ніж гиперкоагуляция, пов'язана з адаптацією гемостазу при фізіологічно протікає вагітності. Дані зміни, що визначають гіперактивність гемостазу в цілому в I тріместере вагітності не розглядається як патологічна активація внутрішньосудинного тромбоутворення, тому що надзвичайно рідко при цьому терміні вагітності ми спостерігали появу маркерів ДВС - продуктів деградації фібрину і фібриногену (ПДФ). Зміст ПДФ в I триместрі не перевищувало 2x10 г / л. Це стало підставою розцінювати гіперактивність тромбоцитарного і плазмового ланок гемостазу, як не відповідає терміну вагітності гиперкоагуляцию і фон для розвитку ДВС.
У II триместрі вагітності, незважаючи на терапію, відзначені зміни в плазмовому ланці гемостазу. Виявлено, що АЧТЧ на 10% і АВР на 5% коротше, ніж при фізіологічній вагітності. Ці дані свідчать про наростаючу гіперкоагуляції. Ця ж тенденція відзначена за тромбоцитопенія еластограмме: показники хронометричні коагуляції r + k, параметри Ма і величини ІТП вище, ніж при фізіологічній вагітності.
У тромбоцитарном ланці гемостазу відзначається статистично достовірне збільшення агрегації і збільшення гіперфункціонального типів кривих при впливі слабкими стимуляторами, що свідчить про стійку гіперактивності тромбоцитів у вагітних з АФС, резистентної до терапії, що проводиться.
У III триместрі вагітності відзначена та ж тенденція до наростання явищ гіперкоагуляції, незважаючи на проведену терапію. Показники концентрації фібриногену, АВР і АЧТЧ, свідчать про розвилася гіперкоагуляції. Хоча в зв'язку з великим контролем гемостазіограми лікувальними заходами вдається утримати гиперкоагуляцию в межах, близьких до фізіологічних параметрів.
З огляду на, що основні, природні інгібітори згортання крові синтезуються судинною стінкою, в тому числі судинами плаценти, великий інтерес представляє оцінка сумарної активності інгібітора активатора плазміногену (ІАП) у міру прогресування вагітності у жінок з антифосфоліпідним синдромом. Проведені в динаміці вагітності визначення змісту ІАП показали, що у вагітних з антифосфоліпідним синдромом відсутній підвищення блокуючого дії ІАП 1 і плацентарного ІАП 2.
Максимальне підвищення інгібітора активатора плазміногену в окремих спостереженнях склало 9,2-9,7 ОД / мл (в нормі цей показник становить 0,3-3,5 ОД / мл) на тлі досить високої активності та вмісту плазміногену - основного фибринолитического субстрату (112 -115% і 15,3-16,3 г / л, при нормі відповідно 75-150% і 8 г / л). Ранні ознаки патологічної активності системи гемостазу (тромбінеміі) в I триместрі за рівнем неактивного комплексу антитромбіну III (TAT) відзначені лише в поодиноких спостереженнях, що підтверджує фактичну внутрисосудистую генерацію прокоагулянтной активності.
Дослідження компонентів противосвертиваючих механізмів системи гемостазу дозволили встановити велику варіабельність вмісту протеїну С (ПРС), в більшості спостережень зниження його рівня не залежить від терміну вагітності. Максимальна активність ПРС не перевищувала 97%, в більшості спостережень - 53-78% (норма 70-140%).
Індивідуальний аналіз змісту інгібітору активатора плазміногену в II триместрі вагітності дозволив виявити різке збільшення інгібітора активатора плазміногену до 75 ОД / мл тільки в 1 випадку, при цьому було поєднання підвищення інгібітора активатора плазміногену з вираженою патологією AT III, активність 45,5%, концентрація 0,423 г / л. У всіх інших спостереженнях зміст інгібітору активатора плазміногену коливалося від 0,6-12,7 ОД / мл, в середньому 4,7 ± 0,08 ОД / мл. Далі, в III триместрі зміст інгібітору активатора плазміногену також була низькою, коливання становили від 0,8 до 10,7 ОД / мл, в середньому 3,2 ± 0,04 ОД / мл, тільки в одному спостереженні - 16,6 ОД / мл. З огляду на, що зазвичай різке збільшення вмісту інгібітору активатора плазміногену сприяє зниженню фібринолітичноїактивності і локальному тромбоутворення (за рахунок придушення репаративного фібринолізу), відмічені нами факти можна розглядати як відсутність реакції ендотелію у вагітних з АФС, спрямованої на синтез ендотеліального компонента ІАП 1, синтезованого ендотелієм судинної стінки, і, що більш важливо, відсутність системи плацентарного компонента ІАП 2, що виділяється судинами плаценти. Можливим поясненням зазначених нами факторів може бути порушення функції ендотеліальних клітин і, в першу чергу, судин плаценти у вагітних з антифосфоліпідним синдромом, ймовірно, за рахунок фіксації на ендотелії комплексів антиген-антитіло.
Звертає на себе увагу значне зниження активності ПРС в II триместрі вагітності на 29% нижче, ніж у контрольній групі.
Оцінка фібринолітичної системи показала наступні результати: активність плазміногену в більшості спостережень була високою в I триместрі 102 ± 6,4% і концентрація 15,7 ± 0,0Ег / л; в II триместрі активність плазміногену була схильна до ще більших коливань від 112до 277% і концентрація від 11,7 г / л до 25,3 г / л, в середньому 136,8 + 11,2% концентрація 14,5 + 0,11 г / л. У III триместрі збереглися аналогічні стану: активність плазміногену коливалася від 104 до 234% (норма 126,8 ± 9,9%) концентрація від 10,8до 16,3 г / л, в середньому 14,5 + 0,11 г / л . Таким чином, фібринолітичний потенціал у вагітних з антифосфоліпідним синдромом досить високий.
На противагу цьому зміст основного інгібітору фібринолізу альфа2-макроглобулин (альфа 2Мд) було досить високим в I триместрі вагітності, коливалося від 3,2 до 6,2 г / л (в нормі 2,4 г / л), в середньому 3,36 ± 0,08 г / л; в II триместрі відповідно від 2,9 до 6,2 г / л, в середньому 3,82 ± 0,14 г / л.
Аналогічні дані отримані щодо змісту альфа1-антитрипсину (альфаlAT), яке в усі триместри вагітності становила від 2,0 до 7,9 г / л. Оскільки CL-Mg і a1-AT відносяться до буферних інгібіторів уповільненої і непрямої дії, їх вплив на активацію фібринолітичної системи, навіть в умовах високого вмісту плазміногену, проявилося зниженням фибринолитического потенціалу у вагітних з антифосфоліпідним синдромом, аналогічне такому при фізіологічному перебігу вагітності.
Перераховані особливості системи гемостазу підкреслюють велику значимість контрольних досліджень гемостазу при вагітності для оптимізації противотромботическое терапії та профілактики ятрогенних ускладнень.
Дослідження системи гемостазу перед пологами показало, що залишається збереженим ГЕМОСТАТИЧНИЙ потенціал і незважаючи на антиагрегантну терапію зберігається тенденція до гіперфункції тромбоцитів.
З огляду на, що пацієнтки з антифосфоліпідним синдромом в процесі вагітності отримують антитромботичні засоби, а після пологів є великий ризик тромбемболіческіх ускладнень, властивих хворим з антифосфоліпідним синдромом, надзвичайно актуальним є дослідження гемостазу в післяпологовому періоді.
Недооцінка гемостазіограми, припинення терапії відразу після пологів може вести до швидко розвивається гіперкоагуляції і тромбемболіческім ускладнень. Дослідження показали, що після пологів залишається високим потенціал згортання крові, навіть в тих спостереженнях, де пацієнтки отримували гепаринотерапии. Дослідження системи гемостазу доцільно проводити на 1, 3 і 5 добу після пологів. Відзначено помірна гіперкоагуляція у 49% породіль, а у 51% породіль відзначена активація системи гемостазу - наростання гіперкоагуляції і поява ПДФ.
Вроджені дефекти гемостазу
В даний час приділяється велика увага генетично детермінованим формам тромбофилии, які подібно антифосфоліпідний синдром супроводжуються тромбоемболічними ускладненнями при вагітності і ведуть до втрати вагітності на будь-якому її етапі. Основні причини спадкової тромбофілії: дефіцит антитромбіну, протеїну С і S, гепарин-кофактора Н, дефіцит фактора ХІІ, дис- і гіпоплазміногенемія, дісфібріногенемія, дефіцит тканинного активатора плазміногену, Лейденовская мутація гена V фактора згортання крові.
Крім цих порушень в останні роки відносять до спадкових тромбофіліческіе станів гіпергомоцистеїнемію - стан, при якому через спадкового дефекту ензиму метилентетрагідрофолат-редуктази є ризик розвитку венозних і артеріальних тромбозів і в зв'язку з цим - втрата вагітності з можливим раннім розвитком еклампсії. Слід зазначити, що в одній з останніх публікацій відзначено, що гіпергомоцистеїнемія виявлена у 11% популяції європейців. На відміну від інших спадкових дефектів гемостазу при цій патології спостерігаються ранні втрати вагітності вже в I триместрі. При гіпергомоцистеїнемії досить ефективною профілактикою тромбозів є застосування фолієвої кислоти.
При виявленні вагітних з спадковими тромбофілії необхідна дуже уважна оцінка даних анамнезу сім'ї. При наявності в анамнезі у найближчих родичів тромбоемболічнихускладнень в молодому віці, при вагітності, при вживанні гормональної терапії, в тому числі, оральних контрацептивів, необхідно обстеження на спадкові дефекти гемостазу, при яких надзвичайно високий ризик тромбоемболічних ускладнень.
Антитромбін інактивує тромбін, фактори IXa, Xa, XIa і ХПА. Дефіцит альфа 1 антитромбіну високо тромбогенний і дає до 50% випадків тромбозів при вагітності. У зв'язку з гетерогенністю порушень частота розповсюдженості цього дефекту варіює від 1: 600 до 1: 5000.
Протеїн С інактивує фактори Va і VIIIa. Протеїн S діє як кофактор протеїну С, посилюючи його дію. Дефіцит протеїну С і S зустрічається з частотою 1: 500. Протеїн С при вагітності практично не змінюється, протеїн S знижується в другій половині вагітності і повертається до норми незабаром після пологів. Тому, якщо визначення протеїну S буде проводитися при вагітності, можна отримати помилково-позитивні результати.
В останні роки багато публікацій про тромбофилии внаслідок мутації гена V фактора, це - так звана Лейденовская мутація. В результаті цієї мутації протеїн С не впливає на V фактор, що і веде до тромбофілії. Цю патологію находяту 9% європейської популяції. Ця мутація повинна бути підтверджена дослідженням ДНК для фактора V Leiden. Частота народження Лейденовской мутації значно варіює. Так, за даними шведських дослідників, частота розповсюдженості цього дефекту гемостазу серед вагітних з тромбозами склала від 46 до 60%, в той час як в Англії - тільки 14% і в Шотландії - 8%.

ПАТОФІЗІОЛОГІЯ СИСТЕМИ ГЕМОСТАЗУ
Значення системи гемостазу
1. Збереження крові в рідкому стані (адекватне співвідношення активності іантизсідальної систем)
2. Попередження і зупинка кровотечі (підтримання постійного об'єму циркулюючої крові)

ВИДИ ГЕМОСТАЗУ
Судинно-тромбоцитарний
(ПЕРВИННИЙ)
- ЗУПИНКА КРОВОТЕЧІ В мікросудин
кОАГУЛЯЦІЙНОГО
(ВТОРИННИЙ)
ФОРМУВАННЯ фібриновими згустки

КОМПОНЕНТИ СИСТЕМИ ГЕМОСТАЗУ
* судинна СТЕНКА
* ТРОМБОЦИТИ (Моноцити, еритроцити)
* ПЛАЗМОВІ СИСТЕМИ:
- прокоагулянти
- АНТИКОАГУЛЯНТИ
- фІБРИНОЛІТИЧНОЇ
- калікреїн-кінінової

КЛАСИФІКАЦІЯ ПОРУШЕНЬ ГЕМОСТАЗУ
ЗА етіології
- СПАДКОВІ
- НАБУТІ
ЗА МЕХАНІЗМОМ РОЗВИТКУ
- ПОРУШЕННЯ СУДИННО-ТРОМБОЦИТАРНОЇ
гемостазу
- ПОРУШЕННЯ КОАГУЛЯЦІЙНОГО гемостазу
За направлення ЗМІН
- гіпокоагуляція
- гіперкоагуляція

гипокоагуляцию
Зниження здатності крові згортатися з появою схильності до повторних кровотеч і крововиливи-вам (спонтанним або після незначних травм)

Етіологія
1. ТРОМБОЦИТОПЕНІЯ
2. тромбоцитопатія
3. вазопатій
4. коагулопатія

ТРОМБОЦИТОПЕНІЯ
Патологічний стан яке характеризується зниженням вмісту тромбоцитів у крові (Менше 150 · 109 / л)

СПАДКОВА ТРОМБОЦИТОПЕНІЯ
Як правило, одновремен-но супроводжується врож-Денн дефектами тромбоцитів

Придбання ТРОМБОЦИТОПЕНІЯ (КЛАСИФІКАЦІЯ ЗА МЕХАНІЗМОМ РОЗВИТКУ)
ПОШКОДЖЕННЯ ТРОМБОЦИТІВ
- імунно комплексами
- механічна травматизація (спленомегалія, гемангіома)
Пригнічення утворення ТРОМБОЦИТІВ
(Апластична анемія, хімічне і радіаційне пошкодження червоного кісткового мозку, заміщення кровотворної тканини пухлиною)
ПІДВИЩЕНИЙ ВИКОРИСТАННЯ ТРОМБОЦИТІВ
(Тромбоз, ДВС-синдром)

ІМУННА ТРОМБОЦИТОПЕНІЯ
гетероіммунние
* Виникає частіше у дітей
** Причина - зміна антигенної структури тромбоцитів (при осіданні вірусів краснухи, віспи, аденовірусів; гаптенов медикаментозного походження - хінідин, сульфаніламіди, рифампіцин; вакцини)
***перебіг сприятливий (При усуненні причини наступає повне одужання)

ІМУННА ТРОМБОЦИТОПЕНІЯ
аутоімунні
Виникає частіше у дорослих
Причина - відсутність імунної толерантності-ності до антигенів власних тромбоцитів
Провокуючі фактори: ліки, віруси, бактерії

аутоіммунна тромбоцитопенія
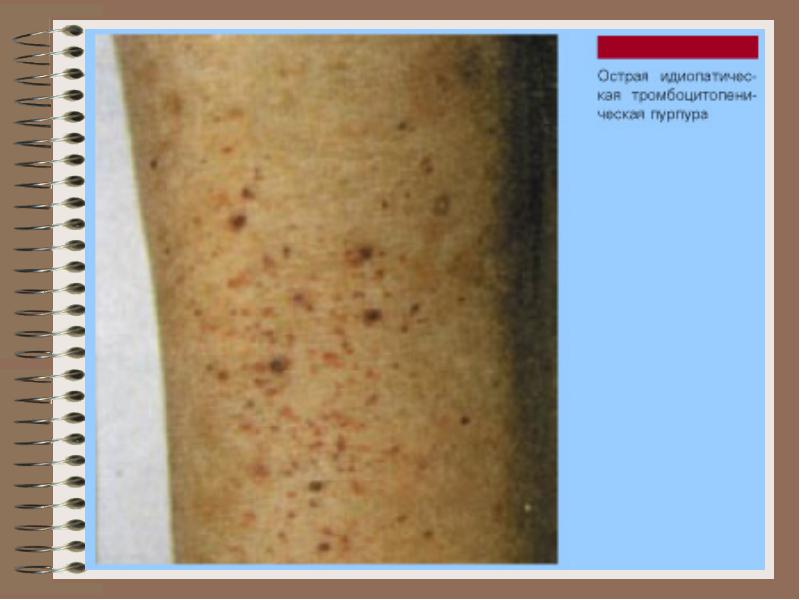
хвороба Верльгофа
(Аутоімунна хронічна тромбоцитопенічна пурпура)
* На поверхні тромбоцитів кількість Ig G збільшується в 10 разів
* Основним місцем синтезу Ig G є селезінка
* принцип лікування:
- спленектомія
- кортикостероїди
- імунодепресантів
* Повного одужання не буває

тромбоцитопатія
Порушення гемостазу внаслідок якісної неповноцінності або дисфункції тромбоцитів, яке характеризується порушенням судинно-тромбоцитарного гемостазу, появою кровоточити-вості тканин і органів

БЕЗ ПОРУШЕННЯ РЕАКЦІЇ ЗВІЛЬНЕННЯ ГРАНУЛ
тромбастенія Гланцмана
* Спадкування - аутосомно-рецесивне
*Причина - відсутність глікопротеїдів 2в і 3а в оболонці тромбоцитів
*патогенез- тромбоцити НЕ взаємодій-обхідних з фібриногеном і не агрегує
*ознаки: петехії, носові кровотечі, маткові кровотечі ( можуть бути смертельними !!)

спадкова тромбоцитопатія
З ПОРУШЕННЯМ РЕАКЦІЇ ЗВІЛЬНЕННЯ ГРАНУЛ
спадкування - аутосомно-рецесивне
Причина - порушення активності ціклоксігена-зи, низька активність контрактільних білків
патогенез - відсутність агрегації при взаємодії з колагеном, відсутність звільнення гранул
ознаки:

спадкова тромбоцитопатія
З ПОРУШЕННЯМ нагромадження та ЗВІЛЬНЕННЯ ВМІСТУ ГРАНУЛ
Хвороба Херджманского-Пудлака (АР)
* Причина - порушення накопичення щільних гранул (АДФ, адреналін, серотонін, Са 2+)
* патогенез - відсутня агрегація при взаємодій-наслідком з колагеном, відсутнє звільнення вмісту гранул
* ознаки: петехії, носові кровотечі, маткові кровотечі

спадкова тромбоцитопатія
З ПОРУШЕННЯМ АДГЕЗІЇ І агрегації тромбоцитів
Синдром Віллебранда-Юргенса (АР)
Причина - дефіцит фактора Віллебранда
патогенез - порушена адгезія тромбоцитів внаслідок дефіциту фактора 8
Хвороба Бернара Сульє (АР)
Причина - відсутність гликопротеида 1 на тромбоцитах
патогенез - порушено взаємодія тромбоцитів з фактором Віллебранда, ф. 5, ф. 11
ознаки - капілярні кровотечі ( особливо небезпечні при статевому дозріванні або пологах)

спадкова тромбоцитопатія
ДЕФІЦИТ І ЗНИЖЕНА ДОСТУПНІСТЬ ф.3
Тромбоцитопатія Боуе і Овена
Причина - дефіцит ф.3 тромбоцитів
патогенез - відсутня взвємодействіе тромбоцитів і прокоагулянтов
ознаки: петехії, носові кровотечі, маткові кровотечі

спадкова тромбоцитопатія
Тромбоцитопатії в поєднанні з іншої спадковими аномаліями
Синдром Віскотта-Олдріджа
- Причина - в тромбоцитах мало щільних гранул (АДФ, серотонін, адреналін, Са2 +), альфа-гранул (бета-тромбоглобуліна, фібриноген, фібронектин, ростовий фактор)
- патогенез -зниженням адгезія і агрегація тромбо-цитов, порушено звільнення гранул
- ознаки:геморагічний синдром появляєтся рано, можуть бути смертельні кровотечі

Придбана тромбоцитопатія (Етіологія)
1. лейкози- мало гранул в тромбоцитах внаслідок прискореного дозрівання, знижена адгезія і агрегація
2. нагромадженняIg М - пошкодження рецепторів імунними комплексами, порушення взаємодії тромбоцитів з прокоагулянти (імунні хвороби)
3. гіповітаміноз В12 - порушено звільнення гранул
4. медикаментозні впливу

медикаментозна тромбоцитопатія
* І нгібітори синтезу тромбоксану А2
-стероідние протизапальні препарати
- нестероїдні протизапальні препарати (аспірин блокує агрегацію тромбоцитів на 4-6 днів)
* Стимулятори освіти цАМФ
-папаверін
-еуфіллін
-анаболіческіе стероїди
* Антагоністи іонів Са
-верапаміл
-корінфар

вазопатій
Геморагічний діатез обумовлений функціональної і морфологічної неполноцен-ністю судинної стінки
- вроджена
- придбана

вроджених вазопатій
Бол. Рандом Ослера (геморагічна телеангіоектазія)
Бол. Фабрі (дифузна ангіокера-томи тулуба)
Спадковий тромбоцитопенія-ний мікроангіоматоз

вроджених вазопатій
Причина - спадкове порушення розвитку сполучної тканини, в т.ч. субендотелія судин
характеристика
- осередкове витончення судин
- розширення просвіту мікросудин
- мало колагенових волокон в субендотеліі
- судини легко травміруються
- Слабкий адгезія і агрегація тромбоцитів внаслідок дефіциту колагенових волокон
**ознаки - кровотечі носові, легенево-бронхіальні та шлунково-кишкові (бувають смертельні)

придбання вазопатій
1. І діопатіческая (Саркома Капоши)
- етіологія - невідома
2. застійна (Дерматит Клотца, дерматит Фавра-черепашки)
- етіологія - хр.сердечная недостатність, локальна венозна недостатність
3. дистрофічна
Стероїдна пурпура - гіперфункція надниркових залоз, лікування кортикостероїдами - пригнічують синтез колагену
Скорбут - дефіцит витий.З
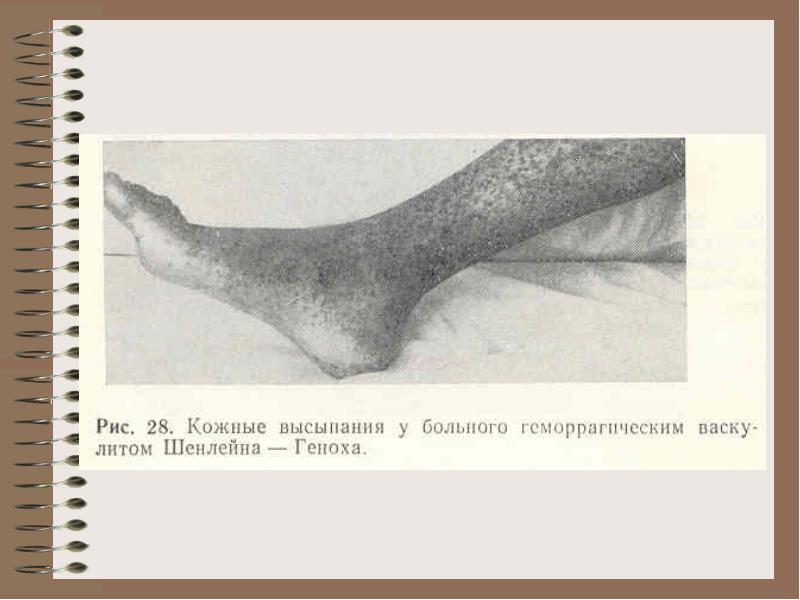
Бол.Шенляйн-Геноха - пошкодження судин імунними комплексами
4. неврогенна
Клінічні ознаки - шкірні форми кровоточивості

коагулопатія
Геморагічний діатез, який виникає в результаті патології коагуляционной системи гемостазу
** спадкова
** придбана

СПАДКОВА коагулопатія
Генетично обумовлене порушення згортання крові внаслідок дефіциту або молекулярної аномалії речовин, що відповідають за коагуляційний гемостаз

СПАДКОВА коагулопатія
КЛАСИФІКАЦІЯ
1. Коагулопатия внаслідок ізольованого порушення внутрішнього механізму формування протромбіназной активності (гемофілії А, В, С, б.Віллебранда, дефіцит Хагемана)
2. Коагулопатия внаслідок ізольованого порушення зовнішнього механізму формування протромбіназной активності (гіпопроконвертінемія - дефіцит 7 ф.)
3. Комбіноване порушення зовнішнього і внутрішнього механізму формування протромбіназной активності (Парагемофілія - дефіцит 5 ф., Б.Стюарта-Прауера - дефіцит 10 ф.)
4. Порушення кінцевої стадії згортання крові (афібриногенемія)

СТАТИСТИКА
Серед усіх форм коагулопатій страждають:
На гемофілію А 68 - 78%
Б . Віллебранда 9 - 18%
На гемофілію В 6 - 13%
На гемофілію С, Парагемофілія і гіпопроконвертінеміей 1 - 2%
Інші форми - клінічна казуїстика

гемофілія А
Геморагічний діатез, обумовлений наслед-тиментом дефіцитом прокоагулянтной частини фактора 8
Фактор 8 (високомолекулярний білок)
1. Глікопротеїн прокоагулянт (VIII: К)
2. Глікопротеїн, який здійснює адгезію тромбоцитів (VIII: ФВ)
3. Глікопротеїн, що активує адгезію тромбоцитів під впливом ристомицина (VIII: Ркоф)
4. антигенний маркер VIII: К (VIII: К АГ)
5. антигенний маркер VIII: Ркоф (VIII: Ркоф АГ)
Активність VIII: К і VIII: ФВ знижується при зменшенні мультімерной структуриі всього 8 фактора

гемофілія А
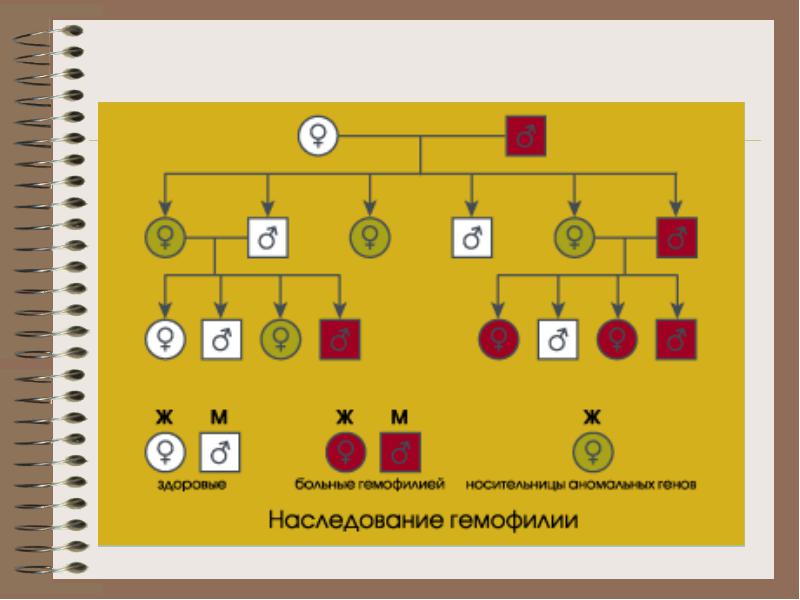
* Е тіологія - аномалія гена в Х-хромосомі, який контролює синтез прокоагулянтной частини ф. 8 (VIII: К)
** Хворіють - чоловіки (46, XhY)
** види
- Гемофілія А + (антигенпозитивних форма - синтезується аномальний VIII: К), Страждають 8 -10%
- Гемофілія А- (антігенотріцательная форма - не синтезується VIII: К), Страждають 90 -92%
**** клініка: крововиливи у великі суглоби, гематоми (підшкірні, внутрішньом'язові), сильні і тривалі посттравматичні кровотечі. Можливі крововиливи-ня до органів черевної порожнини, шлунково-кишкові кровотечі

гемофілія
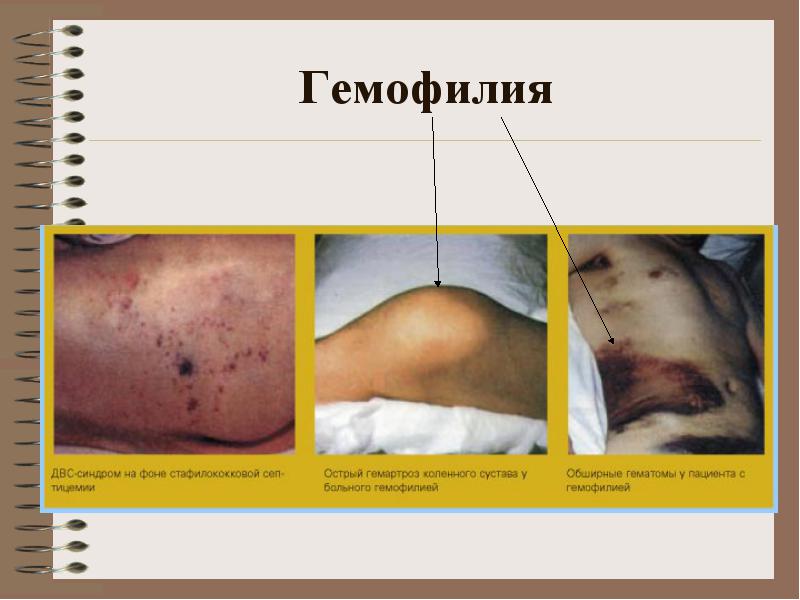
гемофілія
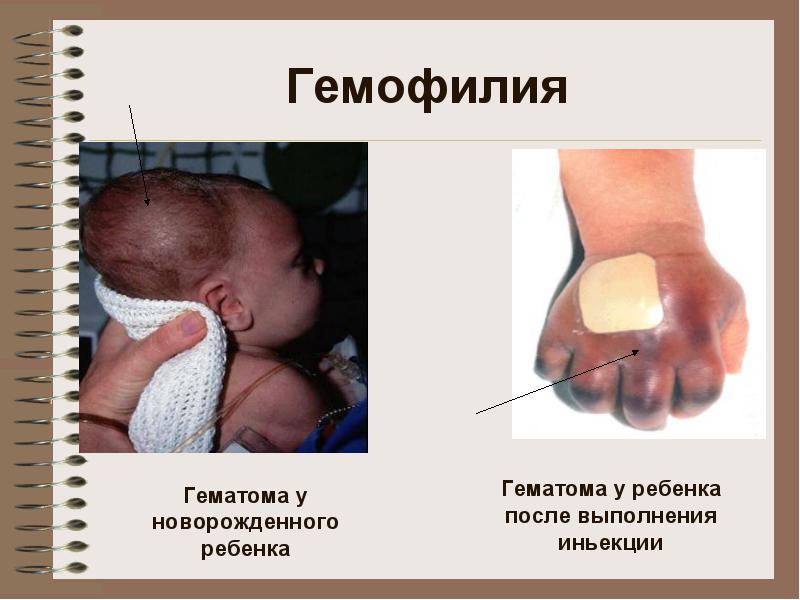
гемофілія В
Етіологія - аномалія гена в Х-хромосомі, який контролює синтез ф. 9
Хворіють - чоловіки (46, XhY)
- жінки (46, XhXh), (45, Xh O)
*** Види
- Гемофілія В + (антигенпозитивних форма - синтезується аномальний ф. 9)
- Гемофілія В- (антігенотріцательная форма - не синтезується ф. 9)
клініка: крововиливи у великі суглоби, гематоми (підшкірні, внутрішньом'язові), сильні і тривалі посттравматичні кровотечі. Можливі крововиливи-ня до органів черевної порожнини, шлунково-кишкові кровотечі

придбання коагулопатія
особливість - полідефіцитна
Етіологія
1. Імунна ингибиция прокоагулянтов (резус конфлікт)
2. Дефіцит віт. К-залежних факторів коагуляції (7, 10, 9, 2)
а) порушення синтезу в кишечнику (дисбактеріоз, пронос)
б) порушення всмоктування віт. К (дефіцит жовчі)
в) тяжке ушкодження печінки
3. Умови та термін гепарину

гіперкоагуляції
Підвищена ЗДАТНІСТЬ КРОВІ утворювати згустки В СУДИНАХ
ТРОМБОЗ
ДВС-СИНДРОМ

ДВС-СИНДРОМ (СИНДРОМ ДЕСІМІНОРОВАННОГО внутрішньосудинного згортання крові)
КЛАСИФІКАЦІЯ
* За клінічним перебігом
1) гострий (миттєві форми характеризуються тяжким перебігом)
2) хронічний
* за поширеністю
1) локалізований
2) генералізований

Етіологія
Інфекції, септичні стани
шок (При септичному - смертність 100%)
Хірургічні втручання, опік
Всі термінальні стани, зупинка серця
Гострий внутрішньосудинний гемоліз
Акушерська патологія (20-25%)
Гемобластози (при о. Лейкозі - 33-45%)
Деструктивні процеси в паренхіматозних органах
алергічні реакції

Стадії ДВС-синдрому
1) Гиперкоагуляция (утворення множинних тромбів внаслідок активації системи коагуляції)
2) Коагулопатия споживання (виснаження системи каогулянтов, надмірне використання тромбоцитопенія цитов для утворення тромбів)
3) Гіпокоагуляція (зниження активності коагу-лянтов, активація антикоагулянтів, активація фібринолізу)
4) Завершення (одужання, ускладнення, смерть)

Патогенез ДВС-синдрому
1) Гіпертромбінемія (Тромбопластин надходить в кров у великій кількості з пошкоджених тканин і спосіб-ствует утворення тромбіну). При інфекціях активовані моноцити-макрофаги синтези-ють власні коагулянти (ф.7, ф.10, ф.9, ф.2)

Патогенез ДВС-синдрому
2) Масивна агрегація тромбоцитів (Викликає розвиток тромбоцітопе-ванні споживання і ускладнюється геморрагиями)
3) Травматизація і гемоліз еритро- цитов (При цьому виділяється багато АДФ, що підсилює адгезію і агрегацію тромбоцитів)

Патогенез ДВС-синдрому
4) "Гуморальний протеазний вибух" (При активації прокоагулянтов, ан-тікоагулянтов, фібринолітиків, білків калікреїн-кінінової системи, системи комплементу в крові накопичується багато продуктів бел-кового розпаду, які є дуже токсичними і пошкоджують судини і тканини)

Патогенез ДВС-синдрому
5) Виснаження системи фибрино-лізу
(Сприяє тромбоутворення)
6) Виснаження факторів згортання крові
(Викликають розвиток геморагій)

Клініка ДВЗ-синдрому
1. Гемокоагуляціонний шок
причина
* Порушення мікроциркуляції (викликають розвиток гіпоксії тканин)
* Накопичення токсичних продуктів протеолізу
прояви
* Зниження артеріального тиску
* Зниження центрального венозного тиску
* Кровотечі (провокують геморагічний шок)

Клініка ДВЗ-синдрому
2. порушення гемостазу
а) гіперкоагуляція
Головний прояв - тромбоз
Кров згортається в пробірці
б) гипокоагуляция
Головний прояв - кровотечі
(Одночасно виснажується система фібринолізу)

Клініка ДВЗ-синдрому
3. тромбоцитопенія
Виникає внаслідок освітньої-ня великої кількості тромбів в судинах (тромбоцитопенія споживання)

У дівчинки після перенесеної ангіни з'явилася петехіальний висип на шкірі кінцівок і тулуб. Об'єктивно: кількість тромбоцитів 80 Г / л, антитромбоцитарні антитіла. Алергічні реакції якого типу (по Кумбсу і Джеллу) лежать в основі цього захворювання?
@ II типу (гуморальні цитотоксические)
I типу (анафілактичні)
III типу (Імунокомплексні)
V типу (стимулюючі)
У хворого порушена адгезія тромбоцитів до колагену і спостерігаються кровотечі з дрібних судин. Порушення якої ланки гемостазу можна допустити у хворого?
@ Судинно-тромбоцитарного
Коагуляційного, І фази
Коагуляційного, ІІІ фази
фібринолізу
Коагуляційного, ІІ фази
У хворого діагностовано тромбоцитопенія. Які клінічні прояви типові для порушень тромбоцитарно-судинного гемостазу?
@ Петехии, екхімози (синці)
гемартрози
гематоми
Зменшення часу кровотечі
Збільшення часу згортання крові
У хворої при обстеженні виявили Тромбоцитопатія. Вкажіть, яке зміна грає важливу роль в патогенезі ТРОМБОЦИТОПАТІЙ?
@ Продукція патологічних тромбоцитів кістковим мозком
Зниження активності антикоагулянтів
гіперактивація тромбоцітопоеза
Підвищення концентрації в крові прокоагулянтов
Пригнічення фібринолізу.
Перед проведенням оперативного втручання виявлено, що у людини час кровотечі збільшено до 10 хв. Дефіцит яких формених елементів в складі крові може бути причиною таких змін?
@ Тромбоцитів
еритроцитів
моноцитів
лімфоцитів
лейкоцитів
У пацієнтки тривале вживання аспірину викликало крововиливи. Об'єктивно: тромбоцитопенія з порушенням функціональної активності тромбоцитів. Тромбоцитопатія в даному випадку викликана пригніченням активності:
@ Циклооксигенази
цитохромоксидази
ліпооксигенази
супероксиддисмутази
Фосфоліпази А 2.
У хворого діагностовано зменшення продукції ендотелієм судин фактора Віллебранда. Яке порушення судинно-тромбоцитарного гемостазу спостерігається при цьому?
@ Порушення адгезії тромбоцитів
Порушення агрегації тромбоцитів
гиперкоагуляция
Порушення полімеризації фібрину
посилення фибринолиз
У дитини з геморагічним висипом, яка виникла після ГРВІ, діагностовано геморагічний васкуліт (хвороба Шенляйн - Геноха). Алергічні реакції якого типу (по Кумбсу і Джеллу) лежать в основі цього захворювання?
@ III типу (Імунокомплексні)
I типу (анафілактичні)
II типу (гуморальні цитотоксические)
IV типу (клітинні цитотоксичні)
V типу (стимулюючі)
У дитини з геморагічним висипом, яка виникла після ГРВІ, діагностовано геморагічний васкуліт (хвороба Шенляйн - Геноха). Що викликає порушення гемостазу при цьому захворюванні?
@ Пошкодження судинної стінки
Спадковий дефект сполучної тканини судинної стінки
Спадковий дефіцит антикоагулянтів
пригнічення фібринолізу
Спадковий дефіцит прокоагулянтов
У жінки, яка страждає на жовчнокам'яну хворобу виявлено геморагічний синдром, обумовлений дефіцитом вітаміну К. Який з перерахованих факторів є неповноцінним при гіповітамінозі К?
@ Стюарта - Прауера (ф. X)
фактор Віллебранда
Фібрінстабілізірующій (ф. XIII)
Фібриноген (ф. I)
У пацієнта при обстеженні було виявлено тромбофілія (прискорення процесу згортання крові). Що могло стати причиною порушення?
@ Дефіцит інгібіторів протеолітичних ферментів
Підвищення концентрації простацикліну
Зниження концентрації тромбіну в крові
Підвищення концентрації гепарину в крові
Підвищення концентрації Фібринолізину в крові
У хворого з захворюванням печінки виявлено зниження вмісту протромбіну в крові. Це призведе до порушення перш за все:
@ Другий фази коагуляційного гемостазу
фібринолізу
Третьої фази коагуляційного гемостазу
Судинно-тромбоцитарного гемостазу
Першої фази коагуляційного гемостазу
У хлопчика 7 років, після падіння з велосипеда виник гемартроз колінного суглоба. Введення кріопреципітату і відкачування крові з суглоба призвело до значного поліпшення стану дитини. Про яке захворювання слід думати?
@ Гемофілія А
Геморагічний васкуліт.
тромбоцитопатія
тромбоцитопенія
Ревматоїдний артрит
У хлопчика з вираженим геморагічним синдромом в плазмі крові відсутньої антигемофільний глобулін А (фактор VIII). Яка фаза гемостазу первинно порушена у цієї дитини?
@ Внутрішній шлях активації протромбінази
Ретракция кров'яного згустку
Зовнішній шлях активації протромбінази
Хлопчик страждає на гемофілію. Якими клінічними ознаками виявляються порушення коагуляционное гемостазу?
петехіальними крововиливами
мікрогематурією
Екхімозами (синцями)
Порушенням гостроти зору
@ Гематоми, тривалими кровотечами
У потерпілого в результаті ДТП через деякий час після перенесеної політравми розвинувся синдром дисемінованого внутрішньосудинного згортання крові (ДВС). Який фактор був ініціатором цього ускладнення?
@ Тканинної тромбопластин (ф. III)
Фібриноген (ф. I)
Антигемофільних глобулін А (ф. VIII)
У хворого на гострий панкреатит розвинувся синдром дисемінованого внутрішньосудинного згортання крові (ДВС). Яка речовина була ініціатором цього ускладнення?
@ Трипсин
Фібриноген (ф. I)
Антигемофільних глобулін А (ф. VIII)
Фактор Стюарта - Прауера (ф. X)
Антигемофільних глобулін В (ф. IX)
У хворого з політравмою і гострою нирковою недостатністю, стан ускладнилося внутрішньою кровотечею. Що є головною ланкою патогенезу цієї стадії ДВС - синдрому?
@ Споживання факторів згортання крові
Викид лейкоцитів з депо
тромбоцитоз
Активація протромбінази
пригнічення фібринолізу
У хворого з опікової хворобою як ускладнення розвинувся ДВЗ - синдром. Яку стадію ДВЗ - синдрому можна запідозрити, якщо відомо, що кров хворого згортається менше ніж за 3 хв.?
@ Гіперкоагуляції
гіпокоагуляції
відновлення
латентну
термінальну
У хворого з травмою розвинувся ДВЗ - синдром. Які зміни гемостазу спостерігаються у ІІ фазу ДВС - синдрому?
@ Гіпокоагуляція
Гиперкоагуляция.
фібриноліз
тромбоцитопенія
тромбоцитопатія
У пацієнта після переливання несумісної крові виник ДВС - синдром. Що є головною ланкою в патогенезі цього ускладнення при гемолізі?
@ Надходження в кров внутрішньоклітинних протеаз
Накопичення білірубіну в крові
Надлишок в крові тромбопластина
Надлишок в крові протромбіну
Збільшення вмісту плазміногену
У хворого на тлі хронічної ниркової недостатності розвинувся ДВЗ-синдром. При обстеженні виявлено збільшення часу згортання крові, тромбоцитопенія, підвищення рівня фібрин-мономірних комплексів і продуктів деградації фібрину. Про якій стадії ДВС-синдрому слід думати?
@ гипокоагуляцию
гіперкоагуляції
відновлення
латентну
нестабільну
У хворого на хронічний лімфолейкоз виникли геморагії в результаті розвитку ДВС - синдрому. Які зміни показників периферичної крові будуть спостерігатися при цьому?
@ Гіпокоагуляція, тромбоцитопенія
Еритроцитоз, підвищення в'язкості крові
Тромбоцитоз, зменшення часу згортання крові
Гиперкоагуляция, збільшення агрегації тромбоцитів
Підвищена активність прокоагулянтов
У жінки з сепсисом з'явилося петехіальні крововиливи, в крові зменшився вміст тромбоцитів і фібриногену, з'явилися продукти деградації фібрину. Що може бути причиною зазначених змін?
@ ДВС синдром
лейкопенія
лімфопенія
тромбоцитоз
